Kim loại kiềm
| Kim loại kiềm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ↓ Chu kỳ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 | Lithium (Li) 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 | Sodium (Na) 11 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4 | Potassium (K) 19 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5 | Rubidium (Rb) 37 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 6 | Caesium (Cs) 55 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 7 | Francium (Fr) 87 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Chú thích
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Kim loại kiềm (tiếng Anh: Alkali metal) là một nhóm các nguyên tố hóa học gồm có lithi (Li), natri (Na), kali (K),[a] rubidi (Rb), caesi (Cs)[b] và franci (Fr). Các kim loại kiềm cùng với hydro tạo thành nhóm IA,[c] nằm trong khối nguyên tố s của bảng tuần hoàn. Tất cả các kim loại kiềm đều có electron ngoài cùng nằm ở orbital-s, và do có chung cấu hình electron giúp các nguyên tố này có các tính chất hóa học tương đối giống nhau.[d] Các nguyên tố kim loại kiềm cũng là những ví dụ tốt cho xu hướng biến đổi tuần hoàn trong bảng tuần hoàn hóa học, với các nguyên tố thể hiện tính đồng đẳng trong các phản ứng.[5] Nhóm các nguyên tố này cũng thường được gọi là họ lithium (tiếng Anh: lithium family), lấy tên nguyên tố đầu tiên của nhóm này là lithi.
Các kim loại kiềm có ánh kim, mềm, dễ dàng phản ứng ở nhiệt độ và áp suất tiêu chuẩn và dễ nhường đi electron ngoài cùng của nó để trở thành một cation với số oxi hóa +1. Nó có thể được cắt dễ dàng bởi một lưỡi dao nhờ độ mềm của chúng, lộ ra một bề mặt ánh kim nhưng bị rữa ngay sau đó do tác dụng với nước và ôxy (nếu với lithi là nitơ) trong không khí. Do sự dễ phản ứng của chúng, các kim loại kiềm thường được bảo quản trong dầu hỏa để tránh nó bị hỏng khi để trong không khí. Tất cả các kim loại kiềm đều phản ứng với nước, càng kim loại ở các chu kỳ sau càng phản ứng mạnh mẽ hơn - từ đó khiến caesi là nguyên tố phản ứng dễ dàng và mạnh nhất trong nhóm.
Tất cả các kim loại kiềm đều xuất hiện trong tự nhiên dưới dạng hợp chất thay vì dạng đơn chất của chúng, với natri dễ tìm nhất - sau đó là kali, lithi, rubidi, caesi và cuối cùng là franci - vốn rất hiếm do tính phóng xạ mạnh của nó, khi chỉ xuất hiện vài phút trong vết đồng vị phóng xạ như một bước trong chuỗi phân rã trong tự nhiên. Ununenni (Uue) - nguyên tố được dự đoán là nguyên tố tiếp theo trong họ kim loại kiềm vẫn chưa được tổng hợp thành công, dù cho nhiều thí nghiệm tổng hợp đã được thực hiện. Tuy nhiên, Ununenni có thể không phải là kim loại kiềm do hiệu ứng lượng tử, khi mà hiệu ứng này đã giúp dự đoán nhiều tính chất hóa học của các nguyên tố siêu nặng.
Đa số các kim loại kiềm đều có nhiều ứng dụng thực tiễn. Một trong những ứng dụng được biết tới nhiều nhất là việc sử dụng rubidi và caesi trong các đồng hồ nguyên tử, mà đồng hồ nguyên tử của caesi được làm chuẩn cho đơn vị thời gian giây. Các hợp chất của natri cũng có nhiều ứng dụng, mà cụ thể là đèn hơi natri và muối ăn - hợp chất của natri và chlor đã được sử dụng từ lâu. Lithi được sử dụng để làm thuốc điều trị tâm thần hoặc làm anot của các pin lithi. Natri, kali và lithi đều là các nguyên tố khoáng như các chất điện li các dung môi sinh học, và mặc dù các nguyên tố kim loại kiềm khác không phải nguyên tố khoáng - chúng đều có những ảnh hưởng, dù tốt hay xấu lên cơ thể động vật.
Lịch sử
[sửa | sửa mã nguồn]
Các hợp chất của natri đã được biết tới từ thời cổ đại, như muối (hay natri chloride) là gia vị, đồng thời là hàng hóa quan trọng trong các hoạt động của con người, với từ tiếng Anh salt được biến điệu từ từ salary - lấy nguyên gốc từ "salarium", khi mà những người lính La Mã được trả tiền để có thể mua muối ăn.[6] Quặng potash cũng đã được sử dụng từ thời cổ đại, nhưng trong phần lớn chiều dài lịch sử người ta không biết rằng nó không phải là một muối khoáng của natri. Georg Ernst Stahl đã có những bằng chứng từ thí nghiệm thực tiễn, điều đó giúp ông đưa ra ý tưởng về việc công bố sự khác nhau cơ bản giữa các muối của natri và kali vào năm 1702,[7] và Henri-Louis Duhamel du Monceau đã chứng minh sự khác biệt này vào năm 1736.[8] Tuy nhiên, hợp chất cụ thể của kali và natri và trạng thái tự nhiên của hai nguyên tố này vẫn chưa được biết tới khi đó - từ đó cũng khiến Antoine Lavoisier không thêm bất cứ nguyên tố kim loại kiềm nào vào danh sách các nguyên tố hóa học của ông vào năm 1789.[9][10]
Kali nguyên chất được điều chế lần đầu tiên vào năm 1807 tại Anh bởi Humphry Davy, ông làm điều này bằng cách điều chế từ kali hydroxide, sau đó điện phân muối nóng chảy mới bởi pin Volta - dụng cụ mới được phát minh khi đó. Các thử nghiệm điện phân trước đó đều thất bại do khả năng phản ứng mạnh của kali, tuy nhiên thành công này cũng đánh dấu lần đầu tiên kim loại được phân lập bằng phuơng pháp điện phân.[11] Cùng năm, Davy cũng công bố việc ông điều chế natri nguyên chất, cũng với một hóa chất tuơng đuơng là xút bởi một kĩ thuật tuơng đuơng, từ đó công bố nguyên tố mới và định nghĩa hai muối của hai kim loại này hoàn toàn khác nhau.[9][10][12][13]

Petalite (hay LiAlSi4O10) được phát hiện lần đầu tiên vào năm 1800 bởi nhà hóa học người Brasil José Bonifácio de Andrada tại một hầm mỏ trên đảo Utö, Thụy Điển.[14][15][16] Tuy nhiên, phải tới năm 1817, khi phân tích mẫu quặng này, Johan August Arfwedson khi đang làm việc trong phòng thí nghiệm của Jöns Jacob Berzelius mới phát hiện ra sự xuất hiện của một nguyên tố mới.[17][18] Nguyên tố mới này khi tạo thành các hợp chất có các tính chất tương tự như natri và kali, dù cho dạng muối carbonate và hydroxide của nó tan ít hơn trong nước, nhưng lại tạo ra môi trường kiềm mạnh hơn.[19] Berzelius đã đặt tên cho nguyên tố chưa biết này là lithion/lithina, lấy nguyên gốc từ từ λιθoς (chuyển tự: lithios, có nghĩa là hòn đá) trong tiếng Hy Lạp cổ đại, để nhấn mạnh nguồn gốc tìm ra nguyên tố này từ trong các quặng rắn, khác với kali khi được tìm thấy trong tro khi đốt các loài thực vật, hay natri với nồng độ tương đối trong máu động vật. Kim loại bên trong quặng petalite được ông đặt tên là lithium.[15][18][20] Liti, natri và kali đều là một phần trong quá trình tìm ra sự biến đổi tuần hoàn của bảng tuần hoàn, khi chúng cùng nằm trong một bộ ba các nguyên tố chung một nhóm và được Johann Wolfgang Döbereiner chỉ ra những điểm giống nhau về tính chất hóa học vào năm 1850.[21]

Rubidi và caesi là những nguyên tố đầu tiên được phát hiện mới bằng việc sử dụng một máy quang phổ - thiết bị mới được phát minh vào năm 1859 bởi Robert Bunsen và Gustav Kirchhoff.[22] Trong năm tiếp theo, họ tìm ra caesi trong các mẫu nước khoáng từ Bad Dürkheim, Đức. Năm 1861, hai nhà khoa học này tìm ra rubidi trong các mẫu quặng lepidolite.[23] Tên của rubidi và caesi bắt nguồn từ quang phổ phát xạ của chúng, với một đường xạ đỏ của rubidi (lấy từ tiếng Latinh từ rubidus, nghĩa là đỏ đậm hay đỏ chói) và một đường xạ xanh da trời của caesi (lấy từ tiếng Latinh từ caesius, nghĩa là xanh da trời).[24][25]
Khoảng năm 1865, John Newlands xuất bản một ấn bản mà ở đó ông liệt kê các nguyên tố theo chiều tăng dần của nguyên tử khối, cùng với đó là những nguyên tố có tính chất vật lý/hóa học tương tự nhau được xếp vào từng nhóm tám nguyên tố một - ông làm điều này dựa trên những quãng tám của âm nhạc, khi mà các nốt nhạc trong cùng một quãng tám có các tính chất âm tương đồng nhau.[26][27] Ấn bản này của ông liệt kê toàn bộ các nguyên tố kim loại kiềm được biết tới khi đó (từ lithi tới caesi), cùng với đồng, bạc và thali (nguyên tố thể hiện số oxi hóa +1 trong các hợp chất giống với kim loại kiềm) đều được xếp vào một nhóm. Tuy nhiên, ông cũng xếp hydro vào cùng nhóm với các halogen.[21]
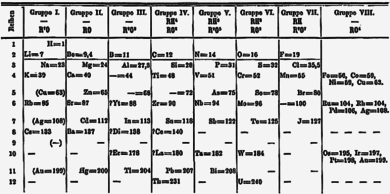
Sau năm 1869, Dmitri Ivanovich Mendeleev trong bảng tuần hoàn hóa học của mình, ông sắp xếp lithi đứng đầu nhóm các nguyên tố với natri, kali, rubidi, caesi và thali.[28] Hai năm sau đó, Mendeleev chỉnh lý lại bảng tuần hoàn của mình, đặt hydro trong cùng nhóm 1 và trước lithi, ông cũng đồng thời chuyển thali xuống nhóm Bor. Trong phiên bản năm 1871, đồng, bạc và vàng xuất hiện tới hai lần, vừa trong nhóm IB, vừa xuất hiện trong "nhóm VII" mà ngày nay trở thành các nhóm từ 8 tới 11.[29][e] Sau khi bảng tuần hoàn gồm 18 cột lần đầu tiên được giới thiệu, nhóm nguyên tố IB được chuyển tới vị trí như hiện của chúng tại khối nguyên tố d, còn các kim loại kiềm được đặt tại nhóm IA. Năm 1988, nhóm này được đổi tên thành nhóm 1. Tên gọi chung "kim loại kiềm" tới từ việc các hydroxide của các nguyên tố trong nhóm 1 này đều tạo ra những môi trường kiềm mạnh khi tan trong nước.[5]
Có ít nhất bốn lần người ta thất bại trong việc phát hiện nguyên tố cuối cùng trong nhóm kim loại kiềm,[30][31][32] trước khi Marguerite Perey thuộc Viện Curie tại Paris, Pháp tìm ra nguyên tố franci vào năm 1939 trong khi tinh chế một mẫu actini-227, được báo cáo có mức năng lượng phân rã là 220 keV. Tuy nhiên, Perey đã phát hiện các hạt phân rã có mức năng lượng dưới 80 keV, khiến bà nghĩ rằng việc phân rã này đã được thực hiện bởi một nhân tố phân rã chưa được biết tới xuất hiện trong quá trình tinh khiết hóa mẫu actini-227. Các thử nghiệm khác nhau đã loại trừ khả năng nhân tố mới này là thori, radi, chì, bismuth hay thali. Sản phẩm mới được sinh ra thể hiện các tính chất hóa học của một kim loại kiềm, điều này khiến Perey tin rằng đây chính là nguyên tố có số hiệu 87, là sản phẩm của quá trình phân rã alpha của actini-227.[33] Sau đó, Perey đã thử nghiệm để xem liệu phân rã beta có tạo ra sản phẩm khác với phân rã alpha hay không, bà đặt nguồn tia alpha ở mức 0,6%, sau này nâng lên 1% theo phương trình:[34]
Nguyên tố tiếp theo sau franci trong bảng tuần hoàn được dự đoán là ununenni (Uue), với số hiệu nguyên tố 119.[35] Các thử nghiệm tổng hợp ununenni lần đầu tiên được thực hiện vào năm 1985 bằng việc bắn phá einsteini-254 bằng ion của calci-48 trong máy gia tốc SuperHILAC tại Berkeley, Carlifornia, tuy nhiên không tạo ra bất cứ nguyên tử nào mới, dẫn tới việc giới hạn vùng phản ứng dưới 300 nb.[36][37]
254
99Es
+ 48
20Ca
→ 302
119Uue
* → không phản ứng[f]
Người ta cho rằng những phản ứng này sẽ không thật sự tạo ra bất cứ nguyên tử ununenni nào trong tương lai gần,[36] gián tiếp khiến cho việc tạo một lượng einsteini-254 vừa đủ để sử dụng cho việc điều chế các nguyên tố siêu nặng trở nên khó khăn hơn do có khối lượng nguyên tử lớn, chu kì bán rã dài 270 ngày, nhưng chỉ có thể được điều chế trong phòng thí nghiệm với lượng nhỏ hơn rất nhiều so với nhu cầu đặt ra.[38] Tuy nhiên, khi mới chỉ có ununenni là nguyên tố chu kì 8 đầu tiên trong bảng tuần hoàn hóa học được mở rộng, nó có thể được tìm ra trong tương lai thông qua các phản ứng khác, và hiện tại đang có những nỗ lực tổng hợp tại Nhật Bản.[39] Cho tới nay, người ta chưa thành công điều chế bất cứ nguyên tố chu kì 8 nào, tuy nhiên giới hạn nuclon cho rằng chỉ có các nguyên tố đầu chu kì 8, có số hiệu nguyên tử dưới 128 mới có thể được điều chế và tồn tại trên phương diện vật lý.[40][41] Chưa có bất cứ thử nghiệm nào được thực hiện để điều chế những nguyên tố kim loại kiềm nặng hơn do số hiệu nguyên tử quá lớn của chúng, và chúng sẽ cần những phương pháp, kĩ thuật mới và mạnh hơn.[35]
Phổ biến
[sửa | sửa mã nguồn]Trong hệ Mặt Trời
[sửa | sửa mã nguồn]
Quy luật Oddo-Harkins cho rằng các nguyên tố với số hiệu nguyên tử chẵn phổ biến hơn các nguyên tố có số hiệu lẻ, với trường hợp ngoại lệ là hydro. Quy luật này cũng khẳng định rằng các nguyên tố với số hiệu nguyên tử lẻ có một proton đơn lẻ và có xu hướng giữ một proton khác, từ đó tăng số hiệu nguyên tử của nó lên thành một số chẵn. Đối với các nguyên tố với số hiệu chẵn, các proton đều bắt cặp, mỗi proton trong cặp thiết lập quỹ đạo quay của proton còn lại, tăng tính bền vững cho nó.[43][44][45] Các kim loại kiềm đều có số hiệu nguyên tử lẻ và không phổ biến như các nguyên tố có số hiệu chẵn kề chúng (nhóm khí trơ và kim loại kiềm thổ) trong hệ Mặt Trời. Các kim loại kiềm nặng hơn cũng ít phổ biến hơn các kim loại nhẹ hơn, như từ rubidi trở đi chỉ có thể được tổng hợp trong các siêu tân tinh mà không thể bởi tổng hợp hạt nhân sao. Lithi cũng có lượng ít hơn natri và kali do được tổng hợp rất ít bởi tổng hợp hạt nhân Big Bang và trong các ngôi sao,
Trong Trái Đất
[sửa | sửa mã nguồn]
Chú thích
[sửa | sửa mã nguồn]Ghi chú
[sửa | sửa mã nguồn]- ^ Kí hiệu nguyên tố Na và K cho natri (sodium) và kali (potassium) được lấy từ tên gốc tiếng Latin của nguyên tố.
- ^ Caesium là tên gọi được đề xuất bởi IUPAC.[1]Cộng đồng Hóa học Hoa Kỳ (ACS - American Chemical Society) đã sử dụng tên gọi caesium từ năm 1921,[2][3]
- ^ Trong quá khứ, cả hệ thống của IUPAC và CAS trong việc đánh số nhóm đều gọi đây là nhóm IA (đọc là nhóm một A, với số I trong hệ Số La Mã).[4]
- ^ Mặc dù hydro cũng có chung kiểu cấu hình electron như vậy, nó không được coi là một kim loại kiềm do thiếu các electron hóa trị ở phân lớp p, từ đó có tính chất hóa học khác biệt.
- ^ Trong phiên bản năm 1869 của bảng tuần hoàn của Mendeleev, đồng và bạc được đặt vào một nhóm riêng của chúng, nối liền với hydro và thủy ngân, còn vàng tạm đặt dưới urani và gali trong nhóm Bor.
- ^ Dấu hoa thị thể hiện trạng thái kích thích
Tham khảo
[sửa | sửa mã nguồn]- ^ International Union of Pure and Applied Chemistry (2005). Danh Pháp Hóa Vô Cơ (IUPAC Hướng dẫn 2005). Cambridge (UK): RSC–IUPAC. ISBN 0-85404-438-8. pp. 248–49. Bản toàn văn..
- ^ Coghill, Anne M.; Garson, Lorrin R. biên tập (2006). The ACS Style Guide: Effective Communication of Scientific Information (ấn bản thứ 3). Washington, D.C.: American Chemical Society. tr. 127. ISBN 978-0-8412-3999-9.
- ^ Coplen, T. B.; Peiser, H. S. (1998). “History of the recommended atomic-weight values from 1882 to 1997: a comparison of differences from current values to the estimated uncertainties of earlier values” (PDF). Pure Appl. Chem. 70 (1): 237–257. doi:10.1351/pac199870010237. S2CID 96729044. Lưu trữ (PDF) bản gốc ngày 9 tháng 10 năm 2022.
- ^ Fluck, E. (1988). “New Notations in the Periodic Table” (PDF). Pure Appl. Chem. IUPAC. 60 (3): 431–436. doi:10.1351/pac198860030431. S2CID 96704008. Lưu trữ (PDF) bản gốc ngày 9 tháng 10 năm 2022. Truy cập ngày 24 tháng 3 năm 2012.
- ^ a b Hội Hóa học Hoàng gia. “Visual Elements: Group 1 – The Alkali Metals”. Visual Elements. Hội Hóa học Hoàng gia. Bản gốc lưu trữ ngày 5 tháng 8 năm 2012. Truy cập ngày 13 tháng 1 năm 2012.
- ^ Harper, Douglas. “salary”. Online Etymology Dictionary.
- ^ Marggraf, Andreas Siegmund (1761). Chymische Schriften (bằng tiếng Đức). tr. 167.
- ^ du Monceau, H. L. D. (1736). “Sur la Base de Sel Marine”. Mémoires de l'Académie Royale des Sciences (bằng tiếng Pháp): 65–68.
- ^ a b Weeks, Mary Elvira (1932). “The discovery of the elements. IX. Three alkali metals: Potassium, sodium, and lithium”. Journal of Chemical Education. 9 (6): 1035. Bibcode:1932JChEd...9.1035W. doi:10.1021/ed009p1035.
- ^ a b Siegfried, R. (1963). “The Discovery of Potassium and Sodium, and the Problem of the Chemical Elements”. Isis. 54 (2): 247–258. doi:10.1086/349704. JSTOR 228541. PMID 14147904. S2CID 38152048.
- ^ Enghag, P. (2004). “11. Sodium and Potassium”. Encyclopedia of the elements. Wiley-VCH Weinheim. ISBN 978-3-527-30666-4.
- ^ Davy, Humphry (1808). “On some new phenomena of chemical changes produced by electricity, in particular the decomposition of the fixed alkalies, and the exhibition of the new substances that constitute their bases; and on the general nature of alkaline bodies”. Philosophical Transactions of the Royal Society of London. 98: 1–44. doi:10.1098/rstl.1808.0001.
- ^ Shaposhnik, V. A. (2007). “History of the discovery of potassium and sodium (on the 200th anniversary of the discovery of potassium and sodium)”. Journal of Analytical Chemistry. 62 (11): 1100–1102. doi:10.1134/S1061934807110160. S2CID 96141217.
- ^ Ralph, Jolyon; Chau, Ida (24 tháng 8 năm 2011). “Petalite: Petalite mineral information and data”. Truy cập ngày 27 tháng 11 năm 2011.
- ^ a b Winter, Mark. “WebElements Periodic Table of the Elements | Lithium | historical information”. Truy cập ngày 27 tháng 11 năm 2011.
- ^ Weeks, Mary (2003). Discovery of the Elements. Whitefish, Montana, United States: Kessinger Publishing. tr. 124. ISBN 978-0-7661-3872-8. Truy cập ngày 10 tháng 8 năm 2009.[liên kết hỏng]
- ^ “Johan Arfwedson”. Bản gốc lưu trữ ngày 5 tháng 6 năm 2008. Truy cập ngày 10 tháng 8 năm 2009.
- ^ a b van der Krogt, Peter. “Lithium”. Elementymology & Elements Multidict. Truy cập ngày 5 tháng 10 năm 2010.
- ^ Clark, Jim (2005). “Compounds of the Group 1 Elements”. chemguide. Truy cập ngày 10 tháng 8 năm 2009.
- ^ Krebs, Robert E. (2006). The History and Use of Our Earth's Chemical Elements: A Reference Guide. Westport, Conn.: Greenwood Press. ISBN 978-0-313-33438-2.
- ^ a b Mark R, Leach. “The Internet Database of Periodic Tables”. meta-synthesis.com.
- ^ Kaner, Richard (2003). “C&EN: It's Elemental: The Periodic Table – Cesium”. American Chemical Society. Truy cập ngày 25 tháng 2 năm 2010.
- ^ Kirchhoff, G.; Bunsen, R. (1861). “Chemische Analyse durch Spectralbeobachtungen” (PDF). Annalen der Physik und Chemie. 189 (7): 337–381. Bibcode:1861AnP...189..337K. doi:10.1002/andp.18611890702. Lưu trữ (PDF) bản gốc ngày 9 tháng 10 năm 2022.
- ^ Weeks, Mary Elvira (1932). “The discovery of the elements. XIII. Some spectroscopic discoveries”. Journal of Chemical Education. 9 (8): 1413–1434. Bibcode:1932JChEd...9.1413W. doi:10.1021/ed009p1413.
- ^ “caesium”. Oxford English Dictionary (ấn bản thứ 2). Oxford University Press. tháng 9 năm 2005. (yêu cầu Đăng ký hoặc có quyền thành viên của thư viện công cộng Anh.)
- ^ Newlands, John A. R. (20 tháng 8 năm 1864). “On Relations Among the Equivalents”. Chemical News. 10: 94–95. Lưu trữ bản gốc ngày 1 tháng 1 năm 2011. Truy cập ngày 25 tháng 11 năm 2013.
- ^ Newlands, John A. R. (18 tháng 8 năm 1865). “On the Law of Octaves”. Chemical News. 12: 83. Lưu trữ bản gốc ngày 1 tháng 1 năm 2011. Truy cập ngày 25 tháng 11 năm 2013.
- ^ Mendelejew, Dimitri (1869). “Über die Beziehungen der Eigenschaften zu den Atomgewichten der Elemente”. Zeitschrift für Chemie (bằng tiếng Đức): 405–406.
- ^ Jensen, William B. (2003). “The Place of Zinc, Cadmium, and Mercury in the Periodic Table” (PDF). Journal of Chemical Education. American Chemical Society. 80 (8): 952–961. Bibcode:2003JChEd..80..952J. doi:10.1021/ed080p952. Bản gốc (PDF) lưu trữ ngày 11 tháng 6 năm 2010. Truy cập ngày 6 tháng 5 năm 2012.
- ^ Fontani, Marco (10 tháng 9 năm 2005). “The Twilight of the Naturally-Occurring Elements: Moldavium (Ml), Sequanium (Sq) and Dor (Do)”. International Conference on the History of Chemistry. Lisbon. tr. 1–8. Bản gốc lưu trữ ngày 24 tháng 2 năm 2006. Truy cập ngày 8 tháng 4 năm 2007.
- ^ “Education: Alabamine & Virginium”. Time. 15 tháng 2 năm 1932. Bản gốc lưu trữ ngày 30 tháng 9 năm 2007. Truy cập ngày 1 tháng 4 năm 2007.
- ^ MacPherson, H. G. (1934). “An Investigation of the Magneto-Optic Method of Chemical Analysis”. Physical Review. American Physical Society. 47 (4): 310–315. Bibcode:1935PhRv...47..310M. doi:10.1103/PhysRev.47.310.
- ^ Adloff, Jean-Pierre; Kaufman, George B. (25 September 2005). Francium (Atomic Number 87), the Last Discovered Natural Element Lưu trữ 4 tháng 6 2013 tại Wayback Machine. The Chemical Educator 10 (5). Retrieved 26 March 2007.
- ^ “Francium”. McGraw-Hill Encyclopedia of Science & Technology. 7. McGraw-Hill Professional. 2002. tr. 493–494. ISBN 978-0-07-913665-7.
- ^ a b The chemistry of the actinide and transactinide elements. Lester R. Morss, Norman M. Edelstein, J. Fuger, Joseph J. Katz (ấn bản thứ 3). Dordrecht: Springer. 2006. ISBN 978-1-4020-3598-2. OCLC 262685616.Quản lý CS1: khác (liên kết)
- ^ a b Lougheed, R. W.; Landrum, J. H.; Hulet, E. K.; Wild, J. F.; Dougan, R. J.; Dougan, A. D.; Gäggeler, H.; Schädel, M.; Moody, K. J.; Gregorich, K. E.; Seaborg, G. (1985). “Search for superheavy elements using 48Ca + 254Esg reaction”. Physical Review C. 32 (5): 1760–1763. Bibcode:1985PhRvC..32.1760L. doi:10.1103/PhysRevC.32.1760. PMID 9953034.
- ^ van der Krogt, Peter. “Ununennium”. Elementymology & Elements Multidict. Truy cập ngày 14 tháng 2 năm 2011.
- ^ Schadel, M.; Brüchle, W.; Brügger, M.; Gäggeler, H.; Moody, K.; Schardt, D.; Sümmerer, K.; Hulet, E.; Dougan, A.; và đồng nghiệp (1986). “Heavy isotope production by multinucleon transfer reactions with 254Es”. Journal of the Less Common Metals. 122: 411–417. doi:10.1016/0022-5088(86)90435-2.
- ^ “Hunt for element 119 set to begin”. Chemistry World. 12 tháng 9 năm 2017. Truy cập ngày 9 tháng 1 năm 2018.
- ^ Seaborg, G. T. (tháng 11 năm 2024). “transuranium element (chemical element)”. Encyclopædia Britannica. Truy cập ngày 16 tháng 3 năm 2010.
- ^ Emsley, John (2011). Nature's Building Blocks: An A-Z Guide to the Elements . New York, NY: Oxford University Press. tr. 593. ISBN 978-0-19-960563-7.
- ^ Lodders, Katharina (2003). “Solar System Abundances and Condensation Temperatures of the Elements”. The Astrophysical Journal. 591 (2): 1220–1247. Bibcode:2003ApJ...591.1220L. doi:10.1086/375492.
- ^ Oddo, Giuseppe (1914). “Die Molekularstruktur der radioaktiven Atome”. Zeitschrift für Anorganische Chemie. 87: 253–268. doi:10.1002/zaac.19140870118.
- ^ Harkins, William D. (1917). “The Evolution of the Elements and the Stability of Complex Atoms. I. A New Periodic System Which Shows a Relation Between the Abundance of the Elements and the Structure of the Nuclei of Atoms”. Journal of the American Chemical Society. 39 (5): 856–879. doi:10.1021/ja02250a002.
- ^ North, John (2008). Cosmos an illustrated history of astronomy and cosmology . Univ. of Chicago Press. tr. 602. ISBN 978-0-226-59441-5.
| Nhóm → | 1A | 2A | 3B | 4B | 5B | 6B | 7B | 8B | 8B | 8B | 1B | 2B | 3A | 4A | 5A | 6A | 7A | 8A | |
| ↓ Chu kỳ | |||||||||||||||||||
| 1 | 1 H |
2 He | |||||||||||||||||
| 2 | 3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne | |||||||||||
| 3 | 11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar | |||||||||||
| 4 | 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
35 Br |
36 Kr | |
| 5 | 37 Rb |
38 Sr |
39 Y |
40 Zr |
41 Nb |
42 Mo |
43 Tc |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe | |
| 6 | 55 Cs |
56 Ba |
* |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
85 At |
86 Rn | |
| 7 | 87 Fr |
88 Ra |
** |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 Ds |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 Mc |
116 Lv |
117 Ts |
118 Og | |
| * Họ Lanthan | 57 La |
58 Ce |
59 Pr |
60 Nd |
61 Pm |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
71 Lu | ||||
| ** Họ Actini | 89 Ac |
90 Th |
91 Pa |
92 U |
93 Np |
94 Pu |
95 Am |
96 Cm |
97 Bk |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 No |
103 Lr | ||||
| |||||
|
| Kim loại kiềm | Kim loại kiềm thổ | Họ Lanthan | Họ Actini | Kim loại chuyển tiếp |
| Kim loại yếu | Á kim | Phi kim | Halogen | Khí hiếm |






![{\displaystyle {\ce {^{227}_{89}Ac ->[{α}][{21,77 năm}] ^{223}_{87}Fr ->[{β−}][{22 phút}] ^{223}_{88}Ra ->[{α}][{11,4 ngày}] ^{219}_{86}Rn}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6b750025d3ae9756f15904cf7bd8e9c770b1751c)