Vanadi(III) bromide
Giao diện
| Vanadi(III) bromide | |
|---|---|
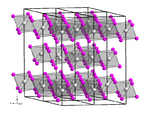 Cấu trúc của vanadi(III) bromide | |
| Danh pháp IUPAC | Vanadium(III) bromide |
| Tên khác | Vanadi tribromide Vanadơ bromide |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| Số RTECS | YW2750000 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| ChemSpider | |
| Thuộc tính | |
| Công thức phân tử | VBr3 |
| Khối lượng mol | 290,653 g/mol (khan) 362,71412 g/mol (4 nước) |
| Bề ngoài | chất rắn màu xám nâu (khan) |
| Khối lượng riêng | 4 g/cm³ |
| Điểm nóng chảy | |
| Điểm sôi | |
| Độ hòa tan trong nước | tan |
| Độ hòa tan | tan trong THF, NH3, CO(NH2)2 (tạo phức) |
| MagSus | +2890,0·10-6 cm³/mol |
| Cấu trúc | |
| Cấu trúc tinh thể | BiI3 |
| Tọa độ | bát diện |
| Các nguy hiểm | |
| Nguy hiểm chính | độ độc cao |
| Các hợp chất liên quan | |
| Anion khác | Vanadi(III) chloride |
| Cation khác | Titan(III) bromide Molybden(III) bromide |
| Hợp chất liên quan | Vanadi(II) bromide Vanadi(IV) bromide |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Vanadi(III) bromide, còn được gọi là vanadi tribromide, là một hợp chất vô cơ có công thức hóa học VBr3. Nó là một polyme với ion bát diện bát giác vanadi(III) được bao quanh bởi sáu phối tử bromide.
Điều chế
[sửa | sửa mã nguồn]VBr3 được điều chế bằng cách xử lý vanadi(IV) chloride bằng hydro bromide:
Phản ứng cũng tạo VBr3 là tiến hành phân hủy vanadi(IV) bromide không ổn định (VBr4), giải phóng Br2 gần nhiệt độ phòng.[1]
Các dung dịch được điều chế từ VBr3 chứa cation trans-[VBr2(H2O)4]+. Sự bay hơi của dung dịch này tạo ra muối trans-[VBr2(H2O)4]Br.[2]
Hợp chất khác
[sửa | sửa mã nguồn]- Giống như VCl3, VBr3 tạo thành các phức màu nâu đỏ tan được trong nước với đimethoxyetan và THF, chẳng hạn như mer-VBr3(THF)3.[3]
- VBr3 còn tạo một số hợp chất với NH3, như VBr3·xNH3 (x = 6, 7) là tinh thể màu nâu sáng.[4][5]
- VBr3 còn tạo một số hợp chất với CO(NH2)2, như VBr3·6CO(NH2)2·3H2O là tinh thể màu lục lam sáng.[6]
Đọc thêm
[sửa | sửa mã nguồn]Stebler, A.; Leuenberger, B.; Guedel, H. U. "Synthesis and crystal growth of A3M2X9 (A = Cs, Rb; M = Ti, V, Cr; X = Cl, Br)". Inorganic Syntheses (1989), tập 26, trang 377–385.
Tham khảo
[sửa | sửa mã nguồn]- ^ Calderazzo, Fausto; Maichle-Mössmer, Cäcilie; Pampaloni, Guido; Strähle, Joachim (1993). “Low-Temperature Syntheses of Vanadium(III) and Molybdenum(IV) Bromides by Halide Exchange”. J. Chem. Soc., Dalton Trans. (5): 655–658. doi:10.1039/DT9930000655.
- ^ Donovan, W. F.; Smith, P. W. "Crystal and Molecular Structures of Aquahalogenovanadium(iii) Complexes. Part 1. X-Ray Crystal Structure of trans-Tetrakisaquadibromovanadium(III) Bromide Dihydrate and the lsomorphous Chloro-compound" Journal of the Chemical Society, Daltor Transactions." 1975, tr. 894–896.
- ^ G. W. A. Fowles, G. W. A.; Greene, P. T.; Lester, T. E. "Ether Complexes of Tervalent Titanium and Vanadium" J. Inorg, Nucl. Chem., 1967. Vol. 29, tr. 2365–2370.
- ^ Vanadium (Leopold Gmelin; Verlag Chemie, 1967), trang 259 – [1]. Truy cập 22 tháng 4 năm 2020.
- ^ Vanadium (Leopold Gmelin; Verlag Chemie, 1967), trang 699 – [2]. Truy cập 12 tháng 5 năm 2020.
- ^ Chemical Abstracts (bằng tiếng Anh). American Chemical Society. 1915. tr. 2852.
