Nguyên tử
| Nguyên tử | ||||||||
|---|---|---|---|---|---|---|---|---|
 | ||||||||
| Hình ảnh minh họa nguyên tử heli, hạt nhân (hồng) và sự phân bố của đám mây electron (đen). Hạt nhân (phía trên bên phải) trong heli-4 thực tế đối xứng cầu và gần giống với đám mây electron, mặc dù đối với những hạt nhân của nguyên tố nặng điều này không hẳn đã đúng. Thanh chuẩn độ lớn là 1 angstrom (10−10 m hay 100 pm). | ||||||||
| Phân loại | ||||||||
| Thành phần nhỏ nhất của nguyên tố hóa học | ||||||||
| Tính chất | ||||||||
|
Nguyên tử là đơn vị cơ bản của vật chất chứa một hạt nhân ở trung tâm bao quanh bởi đám mây điện tích âm các electron (âm điện tử). Hạt nhân nguyên tử là dạng gắn kết hỗn hợp giữa các proton (dương điện tử) mang điện tích dương và các neutron (trung hòa tử) trung hòa điện (ngoại trừ trường hợp của nguyên tử Hydrogen, với hạt nhân ổn định chỉ chứa một proton duy nhất không có neutron). Electron của nguyên tử liên kết với hạt nhân bởi tương tác điện từ và tuân theo các nguyên lý của cơ học lượng tử. Tương tự như vậy, nhóm các nguyên tử liên kết với nhau bởi liên kết hóa học dựa trên cùng một tương tác này, và tạo nên phân tử. Một nguyên tử chứa số hạt electron bằng số hạt proton thì trung hòa về điện tích, trong khi số electron nếu nhiều hoặc ít hơn thì nó mang điện tích âm hoặc dương và gọi là ion. Nguyên tử được phân loại tuân theo số proton và neutron trong hạt nhân của nó: số proton xác định lên nguyên tố hóa học, và số neutron xác định đồng vị của nguyên tố đó.[1]
Tên gọi nguyên tử hóa học mà hay gọi đơn giản là "nguyên tử" là những đối tượng rất nhỏ với đường kính chỉ khoảng vài phần mười nano mét và có khối lượng rất nhỏ tỷ lệ với thể tích của nguyên tử. Chúng ta có thể quan sát nguyên tử đơn lẻ bằng các thiết bị như kính hiển vi quét chui hầm. Trên 99,94% khối lượng nguyên tử tập trung tại hạt nhân,[ct 1] với tổng khối lượng proton xấp xỉ bằng tổng khối lượng neutron. Mỗi nguyên tố có ít nhất một đồng vị với hạt nhân không ổn định có thể trải qua quá trình phân rã phóng xạ. Quá trình này dẫn đến biến đổi hạt nhân làm thay đổi số proton hoặc neutron trong hạt nhân nguyên tử.[2] Electron liên kết trong nguyên tử có những mức năng lượng ổn định rời rạc, hay orbital, và chúng có thể chuyển dịch giữa 2 mức năng lượng bằng hấp thụ hay phát ra photon có năng lượng đúng bằng hiệu giữa 2 mức năng lượng này. Các electron có vai trò xác định lên tính chất hóa học của một nguyên tố, và ảnh hưởng mạnh tới tính chất từ tính của nguyên tử cũng như vật liệu. Những nguyên lý của cơ học lượng tử đã mô tả thành công các tính chất quan sát thấy của nguyên tử và là nền tảng cho lý thuyết nguyên tử và hạt hạ nguyên tử (hạt quark, proton, neutron,...).
Từ nguyên
[sửa | sửa mã nguồn]Tên tiếng Anh "atom" xuất phát từ tiếng Hy Lạp ἄτομος (atomos, "vô hình") từ ἀ- (a-, "không") và τέμνω (temnō, "cắt"),[3] có nghĩa là không cắt được, hoặc vô hình, một thứ không thể chia cắt được.[4] Khái niệm nguyên tử là thành phần vô hình của vật chất do các nhà triết học Ấn Độ và Hy Lạp đề xuất ra đầu tiên. Trong thế kỷ thứ 18 và 19, các nhà vật lý nêu ra một cơ sở vật lý cho ý tưởng này bằng cách chỉ ra có những chất không thể bị bẻ gãy bởi phương pháp hóa học, và họ lấy tên gọi từ các nhà triết học cổ đại là nguyên tử để đặt cho các thực thể hóa học. Trong giai đoạn cuối thế kỷ 19 và đầu thế kỷ 20, các nhà vật lý đã phát hiện ra những thành phần hạ nguyên tử và cấu trúc bên trong nguyên tử, và do vậy chứng minh "nguyên tử" hóa học có thể phân chia được và tên gọi này có thể không miêu tả đúng bản chất của chúng.[5][6] Tuy nhiên, nó đã trở thành một thuật ngữ khoa học hiện đại. Điều này cũng dẫn đến những tranh luận về liệu những nhà triết học cổ đại, những người định nghĩa các vật vô hình và không thể phân chia được có phải là cho những nguyên tử hóa học hiện đại hay là cho những hạt hạ nguyên tử vô hình như lepton hay quark, hay thậm chí cho những hạt cơ bản hơn mà chưa phát hiện ra.[7]
Từ nguyên tử trong tiếng Việt bắt nguồn từ tiếng Hán gốc Nhật 原子 (bính âm: yuánzǐ, tiếng Nhật: genshi). Với nguyên trong nguyên thủy và tử trong phân tử
Lịch sử
[sửa | sửa mã nguồn]Nguyên tử luận
[sửa | sửa mã nguồn]Khái niệm về vật chất là tổ hợp của những đơn vị rời rạc và không thể chia nhỏ hơn đã xuất hiện từ nhiều thiên niên kỷ, nhưng những khái niệm này thường là những lập luận triết học và trừu tượng hơn là dựa trên những quan sát thực nghiệm. Bản chất của nguyên tử trong triết học thay đổi theo thời gian giữa nhiều nền văn minh và trường phái cổ đại, đa số có yếu tố tinh thần siêu hình học. Tuy vậy, khái niệm cơ bản về nguyên tử được các nhà khoa học hàng nghìn năm sau chấp nhận bởi vì nó giải thích một cách đơn giản một số khám phá mới trong lĩnh vực hóa học.[8]

Các nhà triết học cổ đại Hy Lạp và Ấn Độ đã nhắc tới khái niệm nguyên tử. Ở Ấn Độ, những trường phái Ājīvika, Jain, và Cārvāka bàn về nguyên tử luận bắt đầu từ thế kỷ thứ 6 trước Công nguyên.[9] Hệ thống tư tưởng Nyaya và Vaisheshika sau đó phát triển thuyết về nguyên tử khi đề ra cách các nguyên tử kết hợp lại thành thực thể phức tạp hơn.[10] Ở phương Tây, nguyên tử luận được nhắc đến từ thế kỷ 5 TCN bởi Leucippus, và người học trò của Democritos đã tiếp nối và hệ thống hóa lý luận. Khoảng giai đoạn 450 TCN, Democritos đưa ra thuật ngữ atomos (tiếng Hy Lạp: ἄτομος), có nghĩa là "không thể cắt được" hay "hạt vô hình nhỏ nhất của vật chất". Mặc dù các khái niệm này của các triết gia Ấn Độ và Hy Lạp cổ đại thuần túy dựa vào mặt tinh thần, khoa học hiện đại đã bảo lưu thuật ngữ do Democritos đưa ra.[8]
Lý thuyết về những hạt rất nhỏ (Corpuscularianism) do nhà giả kim Geber nêu ra từ thế kỷ XIII,[11] đôi khi có người cho là bởi Paul từ Taranto nêu ra, đó là mọi vật thể chứa bên trong và những hạt hoặc những tiểu thể rất nhỏ.[12] Chủ nghĩa này giống với nguyên tử luận, ngoại trừ nguyên từ được giả thiết là hạt vô hình, và những hạt về nguyên lý có thể phân chia được. Theo lý thuyết này, ví dụ, người ta cho rằng thủy ngân có thể thấm vào kim loại và làm thay đổi cấu trúc bên trong của nó.[13] Corpuscularianism là lý thuyết nổi bật trong vài trăm năm sau đó.
Năm 1661, nhà triết học tự nhiên Robert Boyle xuất bản cuốn The Sceptical Chymist trong đó ông lập luận rằng vật chất là tổ hợp của rất nhiều "tiểu thể" hay nguyên tử, hơn là bởi bốn nguyên tố cơ bản là không khí, đất, nước và lửa.[14] Trong những năm 1670 lý thuyết về các tiểu thể được Isaac Newton áp dụng vào lý thuyết các hạt ánh sáng của ông.[12][15]
Nguồn gốc lý thuyết khoa học
[sửa | sửa mã nguồn]
Tiến trình nghiên cứu về nguyên tử không xuất hiện cho tới tận khi ngành khoa học hóa học bắt đầu phát triển. Năm 1789, thương nhân và khoa học gia người Pháp Antoine Lavoisier khám phá ra định luật bảo toàn khối lượng và nêu ra ý niệm về nguyên tố là chất cơ bản không thể phân tách bằng những phương pháp hóa học.[16]
Năm 1805, nhà triết học và giảng sư người Anh John Dalton sử dụng khái niệm nguyên tử nhằm giải thích tại sao các nguyên tố luôn luôn phản ứng theo những tỉ số tự nhiên nhỏ (định luật Dalton) và tại sao có những loại khí hòa tan vào nước tốt hơn những khí khác. Ông đề xuất rằng mỗi nguyên tố chứa những nguyên tử cùng loại, duy nhất, và những nguyên tử này kết hợp với nhau tạo nên các hợp chất hóa học.[17][18] Các nhà lịch sử khoa học coi Dalton là người tiên phong trong lý thuyết nguyên tử hiện đại.[19]
Giả thuyết nguyên tử của Dalton không nêu cụ thể kích thước nguyên tử là bao nhiêu. Theo cảm nhận thông thường chúng phải rất nhỏ, nhưng không ai biết nhỏ bao nhiêu. Do vậy vào năm 1865 nhà hóa học người Áo Johann Josef Loschmidt đã có bước đột phá khi ông đo được kích cỡ của phân tử trong không khí.[20]
Một dòng bổ sung lý luận hỗ trợ lý thuyết hạt (và do vậy mở rộng thuyết nguyên tử) là vào đầu năm 1827 khi nhà thực vật học Scotland Robert Brown sử dụng kính hiển vi để quan sát các hạt bụi trôi nổi trên mặt nước và ông nhận thấy chúng di chuyển zic-zac—một hiện tượng ngày nay gọi là "chuyển động Brown". Năm 1877 J. Desaulx đề xuất hiện tượng này có nguyên nhân từ chuyển động nhiệt của các phân tử nước, và tới tận năm 1905 nhà vật lý người Đức Albert Einstein mới nêu ra phân tích toán lý đầu tiên về chuyển động này.[21][22][23] Sau đó, nhà vật lý người Pháp Jean Perrin dựa trên nghiên cứu của Einstein tiến hành thí nghiệm xác định được khối lượng và kích thước nguyên tử, và xác nhận lý thuyết nguyên tử của Dalton.[24]

Năm 1869, dựa trên các khám phá trước đó của những nhà khoa học như Lavoisier, nhà hóa học người Nga Dmitri Mendeleev lần đầu tiên công bố bảng tuần hoàn các nguyên tố hóa học.[25] Trên bảng này thể hiện tính chất hóa học một cách tuần hoàn giữa các nguyên tố, ông phát hiện ra tính lặp lại tuần hoàn của các nguyên tố khi sắp xếp chúng theo nguyên tử số.[26]
Hạt cấu thành và lý thuyết lượng tử
[sửa | sửa mã nguồn]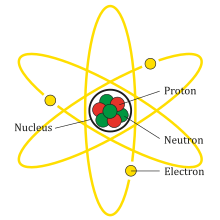
Nhà vật lý J. J. Thomson, thông qua nghiên cứu trên chùm tia cathode năm 1897, đã phát hiện ra electron, và kết luận rằng chúng là một thành phần của mỗi nguyên tử. Do vậy ông vượt qua niềm tin lâu nay cho rằng nguyên tử là những hạt vô hình, không thể phân chia của vật chất.[27] Thomson đề xuất các hạt điện tích âm electron khối lượng nhỏ phân bố đều trên nguyên tử, có thể quay quanh thành những vòng, và điện tích của chúng cân bằng với sự có mặt của một biển điện tích dương. Mô hình này sau đó được gọi là mô hình mứt mận (Plum pudding model).
Năm 1909, Hans Geiger và Ernest Marsden, lúc đó đang là trợ tá cho Ernest Rutherford, sử dụng tia alpha—lúc đó người ta đã biết là nguyên tử điện tích dương của heli—bắn phá một lá vàng và nhận thấy một tỷ lệ nhỏ các hạt bị lệch với một góc rất lớn so với giá trị tiên đoán theo mô hình Thomson. Rutherford giải thích thí nghiệm với lá vàng bằng giả sử rằng điện tích dương của nguyên tử vàng và phần lớn khối lượng của nó tập trung tại hạt nhân trung tâm của nguyên tử—hay mô hình Rutherford.[28]
Khi làm thí nghiệm với các nguyên tố phóng xạ, năm 1913 nhà hóa học phóng xạ Frederick Soddy phát hiện ra dường như có nhiều hơn một loại nguyên tử tại mỗi vị trí trên bảng tuần hoàn.[29] Và thuật ngữ đồng vị do bác sĩ Margaret Todd đưa ra nhằm gọi tên một cách phù hợp cho những nguyên tử khác nhau của cùng một nguyên tố. J.J. Thomson nghĩ ra một kĩ thuật nhằm tách nguyên tử có các đồng vị khác nhau khi ông nghiên cứu trên khí ion hóa, và sau đó dẫn tới khám phá ra đồng vị bền.[30]
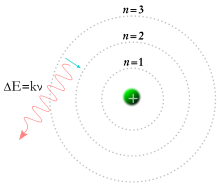
Trong khi đó năm 1913, nhà vật lý Niels Bohr đề xuất là các electron bị giam giữ trên những quỹ đạo bị lượng tử hóa nhất định, và chúng có thể nhảy qua lại giữa những quỹ đạo này, nhưng không thể rơi xoắn ốc vào trong hay ra ngoài trong những quỹ đạo trung gian.[31] Một electron phải hấp thụ hoặc phát ra một lượng năng lượng cụ thể khi chuyển dịch giữa hai trạng thái này. Khi ánh sáng từ nguồn vật liệu nung nóng truyền qua một lăng kính, nó bị tách ra thành phổ nhiều tia đơn sắc. Lý thuyết Bohr đã giải thích thành công sự tách ra thành nhiều vạch phổ hydro tương ứng với sự chuyển dịch electron giữa các orbital.[32]
Sau đấy trong cùng năm Henry Moseley cung cấp thêm chứng cứ thực nghiệm ủng hộ lý thuyết Niels Bohr. Những kết quả thí nghiệm này cũng tinh chỉnh mô hình của Ernest Rutherford và của Antonius Van den Broek, và thí nghiệm cho thấy nguyên tử chứa trong nó hạt nhân có số điện tích hạt nhân bằng với số thứ tự của chúng trên bảng tuần hoàn. Cho đến tận khi có các thí nghiệm của Moseley, nguyên tử số vẫn chưa được biết là một đại lượng vật lý và xác nhận bằng thực nghiệm. Nguyên tử số bằng điện tích của hạt nhân vẫn được chấp nhận trong mô hình nguyên tử hiện đại ngày nay.[33]
Liên kết hóa học giữa các nguyên tử đến lượt được giải thích bởi Gilbert Newton Lewis năm 1916, bằng tương tác giữa các electron trong chúng.[34] Khi đã biết tính chất hóa học của các nguyên tố lặp lại tuần hoàn trên bảng tuần hoàn,[35] năm 1919 nhà hóa học Irving Langmuir đề xuất tính tuần hoàn có thể giải thích được nếu electron trong một nguyên tử được kết nối hay nhóm lại theo một cách nào đó. Nhóm các electron được cho là chiếm giữ vào một tập hợp lớp vỏ electron quanh hạt nhân.[36]
Thí nghiệm Stern–Gerlach thực hiện năm 1922 mang đến kết quả thực nghiệm ủng hộ cho bản chất lượng tử của nguyên tử. Khi một chùm nguyên tử bạc cho phóng qua một từ trường không đều, chùm tia sẽ bị tách ra trên màn thu tuân theo hướng của động lượng nguyên tử, hay spin lượng tử. Nếu hướng của spin là phân bố ngẫu nhiên, thì trên màn thu sẽ thu được một dải bạc liên tục. Tuy vậy, hai nhà vật lý lại thu được kết quả là có hai phần rõ rệt, chỉ phụ thuộc vào spin nguyên tử định hướng lên hay xuống.[37]
Năm 1924, Louis de Broglie dựa trên ý tưởng của Einstein về sóng điện từ có lúc thể hiện tính chất hạt (photon) và đề xuất ngược lại là mọi hạt có tính chất dạng sóng của chúng. Năm 1926, Erwin Schrödinger sử dụng đề xuất này nhằm phát triển mô hình toán học về nguyên tử miêu tả các electron như dạng sóng ba chiều hơn là các hạt điểm. Một hệ quả của cách sử dụng các hàm sóng miêu tả hành xử của hạt đó là về mặt toán học không thể nhận được giá trị chính xác về cả vị trí và động lượng của một hạt trong cùng một thời gian; đây chính là nội dung của nguyên lý bất định do nhà vật lý Werner Heisenberg phát biểu năm 1926. Trong khái niệm này, mỗi khi chúng ta đo chính xác vị trí của hạt chúng ta sẽ chỉ nhận được một khoảng các giá trị có thể cho động lượng, và ngược lại. Mô hình này cũng giải thích được những kết quả thực nghiệm về hành xử của nguyên tử mà những mô hình khác không làm được, như là những cấu trúc xác định và dải phổ của những nguyên tử lớn hơn nguyên tử hydro. Từ đó, mô hình hành tinh nguyên tử miêu tả các electron quay trên quỹ đạo quanh hạt nhân bị bác bỏ và thay thế vào đó là các electron ở những vùng gọi là orbital nguyên tử tương ứng với xác suất phân bố của electron.[38][39]

Các phổ kế khối lượng phát minh ra đã cho phép đo được chính xác khối lượng của nguyên tử. Thiết bị này sử dụng một nam châm làm lệch quỹ đạo của chùm tia ion, và góc lệch đo được bằng tỉ số của khối lượng nguyên tử và điện tích của nó. Nhà hóa học Francis William Aston đã sử dụng thiết bị này để chứng tỏ rằng các đồng vị có khối lượng khác nhau. Khối lượng nguyên tử của những đồng vị cùng một nguyên tố chỉ chênh nhau theo bội nguyên của một hằng số.[40] Để giải thích cho sự khác biệt kỳ lạ về khối lượng đồng vị phải đợi đến tận khi khám phá ra neutron, hạt trung hòa điện có khối lượng hơi lớn hơn khối lượng proton, do nhà vật lý James Chadwick phát hiện năm 1932 khi bắn phá hạt nhân nguyên tử Beryli bằng các hạt alpha. Do vậy các đồng vị được giải thích như là các nguyên tố có cùng số proton và khác nhau về số neutron ở hạt nhân của chúng.[41]
Phân hạch, vật lý năng lượng cao và vật chất ngưng tụ
[sửa | sửa mã nguồn]Năm 1938, nhà hóa học người Đức Otto Hahn, học trò của Rutherford, đã hướng chùm neutron vào các nguyên tử urani nhằm mục đích tạo ra các nguyên tố siêu urani. Thay vào đó ông lại nhận được từ kết quả thí nghiệm hóa học là sản phẩm bari.[42] Một năm sau, Lise Meitner và người cháu trai của Otto Hahn là Otto Frisch xác nhận kết quả Hahn thu được là thực nghiệm đầu tiên về sự phân hạch hạt nhân.[43][44] Năm 1944, Otto Hahn nhận giải Nobel Hóa học. Mặc dù Hahn đã nỗ lực kêu gọi Ủy ban Nobel trao giải cho Meitner và Frisch nhưng ông đã không thành công.[45]
Trong thập niên 1950, với sự phát triển nhanh chóng của các máy gia tốc hạt và máy dò hạt đã cho phép các nhà khoa học nghiên cứu va chạm của các hạt nhân và nguyên tử ở mức năng lượng cao.[46] Họ nhận thấy hạt neutron và proton là những loại hạt hadron, hay hạt tổ hợp của những hạt nhỏ hơn gọi là quark. Lý thuyết Mô hình chuẩn của vật lý hạt được phát triển và đã rất thành công trong giải thích tính chất của hạt nhân theo sự phân loại thành các hạt hạ nguyên tử và các tương tác chi phối thế giới lượng tử.[47]
Các thành phần
[sửa | sửa mã nguồn]Hạt hạ nguyên tử
[sửa | sửa mã nguồn]Mặc dù từ nguyên tử có nguồn gốc chỉ những hạt không thể phân chia nhỏ hơn nữa, nhưng như ngày nay đã biết nguyên tử là thuật ngữ khoa học tổ hợp của nhiều hạt hạ nguyên tử. Các hạt thành phần của nguyên tử là electron, proton và neutron. Ngoại trừ nguyên tử hydro-1 không có neutron và ion hydro không có electron (hay chính là hạt proton đơn lẻ).
Electron là hạt nhẹ nhất trong ba hạt với khối lượng 9,109×10−31 kg, và điện tích âm -e, kích thước của nó rất nhỏ và hiện nay chưa có công nghệ nào đo được đường kính của nó.[48] Proton có điện tích dương +e và khối lượng gấp 1.836 khối lượng electron, và bằng 1,673×10−27 kg, mặc dù giá trị này có thể giảm đi do bù trừ vào năng lượng liên kết của proton trong hạt nhân. Neutron là hạt trung hòa điện và khối lượng khi nó đứng riêng lẻ là 1.839 lần khối lượng electron,[49] hay 1,675×10−27 kg. Các nhà vật lý đo được đường kính của neutron và proton—vào cỡ 25×10−15 m—mặc dù 'bề mặt' của những hạt này không xác định rõ ràng.[50]
Trong Mô hình chuẩn, electron là hạt cơ bản thực sự vì nó không có hạt thành phần. Tuy nhiên, cả proton và neutron là những hạt tổ hợp của những hạt cơ bản gọi là quark. Có hai loại quark trong các proton và neutron, mỗi hạt quark mang điện tích phân số. Proton là hạt tổ hợp của 2 quark lên (mỗi hạt có điện tích +2⁄3e) và một quark xuống (với điện tích −1⁄3e). Neutron chứa một quark lên và hai quark xưống. Sự khác biệt trong thành phần khiến cho khối lượng và điện tích của hai hạt proton và neutron có sự khác nhau.[51][52]
Các quark liên kết với nhau bởi tương tác mạnh (hay lực mạnh) thông qua trao đổi các gluon. Đến lượt các hạt proton và neutron liên kết với nhau trong hạt nhân bởi lực hạt nhân, mà lực này về bản chất là do tương tác mạnh 'rò rỉ' ra ngoài với phạm vi ngắn (xem bài về lực hạt nhân). Hạt gluon là thành viên của họ hạt boson gauge, là hạt trung gian trao đổi tương tác mạnh.[51][52]
Hạt nhân
[sửa | sửa mã nguồn]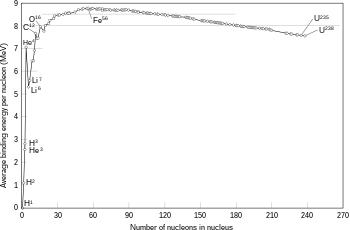
Mọi proton và neutron liên kết với nhau trong hạt nhân nguyên tử, và chúng được gọi chung là các nucleon. Bán kính của hạt nhân có giá trị xấp xỉ 1,07 3√A fm, với A là tổng số nucleon trong hạt nhân.[53] Giá trị này nhỏ hơn rất nhiều bán kính của nguyên tử và bằng khoảng 105 fm. Các nucleon liên kết với nhau bởi thế năng hút còn dư của tương tác mạnh tầm ngắn. Với khoảng cách 2,5 fm lực này mạnh hơn lực điện từ làm cho các proton điện tích dương đẩy nhau.[54]
Các nguyên tử của cùng một nguyên tố có cùng số proton, hay còn gọi là số nguyên tử. Hạt nhân của một nguyên tố có số hạt neutron khác nhau xác định lên các đồng vị của nguyên tố đó. Tổng số proton và neutron xác định lên nuclit. Số lượng tương đối neutron so với proton ảnh hưởng tới tính ổn định của hạt nhân, và ở một số đồng vị có hiện tượng phân rã phóng xạ.[55]
Các hạt proton và neutron được phân loại thành hạt fermion. Nguyên lý loại trừ Pauli, một hiệu ứng cơ học lượng tử, không cho phép có hai hạt fermion đồng nhất ở cùng một trạng thái, ví dụ như không thể có nhiều hạt proton có cùng một trạng thái lượng tử trong cùng một thời gian. Do vậy mỗi hạt proton trong hạt nhân phải có các trạng thái khác nhau, với mức năng lượng của riêng chúng, và tương tự quy tắc này cho các hạt neutron. Tuy nhiên nguyên lý này không ngăn cấm một hạt proton và một neutron có cùng trạng thái lượng tử.[56]
Đối với các nguyên tử có giá trị nguyên tử số thấp, một hạt nhân có số proton khác số neutron có xu hướng trở về trạng thái năng lượng của hạt nhân thấp hơn thông qua quá trình phân rã phóng xạ dẫn đến số hạt proton và neutron trở lên xấp xỉ bằng nhau. Kết quả là, các nguyên tử có số proton xấp xỉ bằng số neutron có hạt nhân bền và không có hiện tượng phóng xạ. Tuy nhiên, khi nguyên tử số tăng lên, lực đẩy lẫn nhau giữa các proton và đòi hỏi số neutron tăng lên để duy trì sự ổn định của hạt nhân, không còn tuân theo xu hướng cân bằng hai hạt này nữa. Và thực tế không có hạt nhân bền nào với số proton xấp xỉ bằng số neutron khi nguyên tử số lớn hơn Z = 20 (calci); và khi Z tăng đến những hạt nhân nặng nhất, tỉ số neutron trên proton để cho hạt nhân ổn định tiến tới giá trị 1,5.[56]
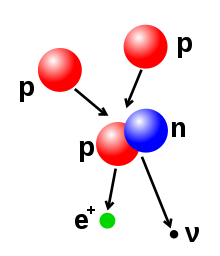
Các nhà khoa học biết hạt nhân nguyên tử có thể thay đổi số proton và neutron, mặc dù sự điều chỉnh này cần năng lượng rất cao do ảnh hưởng của lực hạt nhân cũng như lực điện từ. Phản ứng tổng hợp hạt nhân xảy ra khi nhiều hạt nhân kết hợp lại thành một hạt nhân nặng hơn, như sự va chạm năng lượng cao giữa hai hạt nhân. Ví dụ, tại lõi Mặt Trời các proton đòi hỏi năng lượng cỡ 3–10 keV để vượt qua lực đầy giữa chúng— để vượt qua rào Coulomb—và tổng hợp lại thành hạt nhân nặng hơn.[57] Phản ứng phân hạch hạt nhân là quá trình ngược lại, một hạt nhân bị tách ra làm hai hạt nhân có khối lượng nhỏ hơn—thường thông qua quá trình phân rã phóng xạ. Hạt nhân cũng bị biến đổi do kết quả quá trình bắn phá bởi các hạt hạ nguyên tử hay chùm proton năng lượng cao. Nếu hạt nhân mới sinh ra với số proton khác đi thì nguyên tử trở thành một nguyên tử của nguyên tố hóa học khác.[58][59]
Nếu khối lượng của hạt nhân sản phẩm trong phản ứng tổng hợp nhỏ hơn tổng cộng khối lượng của các hạt nhân tham gia phản ứng, thì hiệu khối lượng này có thể phát ra dưới dạng năng lượng có ích (như tia gamma, hay động năng của các hạt sản phẩm như hạt beta), và tuân theo nguyên lý sự tương đương khối lượng-năng lượng với công thức của Albert Einstein ΔE = Δm.c2, với Δm là khối lượng chênh lệch và c là tốc độ ánh sáng. Năng lượng dôi ra này có nguồn gốc từ năng lượng liên kết của hạt nhân tạo thành, và nó là sự mất mát năng lượng không thể khôi phục được làm cho các hạt tham gia tổng hợp đứng cạnh nhau trong một trạng thái đòi hỏi năng lượng này phải tách ra.[60]
Phản ứng tổng hợp tạo ra hạt nhân lớn hơn từ các hạt nhân có nguyên tử số Z nhỏ hơn của sắt và nikel – với tổng số nucleon vào khoảng 60—thường là phản ứng sinh nhiệt giải phóng nhiều năng lượng hơn so với năng lượng cần thiết để tổng hợp chúng.[61] Đây chính là những phản ứng tổng hợp hạt nhân sinh năng lượng trong các sao và giúp ngôi sao duy trì trạng thái cân bằng áp suất và lực hút hấp dẫn. Đối với các hạt nhân nặng hơn, năng lượng liên kết trên một nucleon trong hạt nhân bắt đầu giảm. Điều này làm cho phản ứng tổng hợp sinh ra hạt nhân với nguyên tử số Z > 26 và số nucleon cao hơn 60, là phản ứng thu nhiệt. Những hạt nhân nặng này không thể tham gia phản ứng tổng hợp sinh năng lượng giúp cho quá trình cân bằng thủy tĩnh của sao được ổn định.[56]
Đám mây electron
[sửa | sửa mã nguồn]
Các electron trong một nguyên tử bị hút bởi các proton ở hạt nhân bằng lực điện từ. Lực này giam các electron bên trong một giếng thế tĩnh điện bao quanh hạt nhân, tức là cần phải có nguồn năng lượng từ bên ngoài để cho electron thoát ra khỏi hạt nhân. Electron càng nằm gần về phía hạt nhân, lực hút càng mạnh hơn. Do đó electron liên kết gần tâm của giếng thế đòi hỏi nhiều năng lượng hơn để thoát ra ngoài.
Electron, giống như những hạt vi mô khác, có cả tính chất sóng và hạt. Đám mây electron là một vùng bên trong giếng thế nơi mỗi electron tạo thành một kiểu sóng đứng ba chiều – dạng sóng không di chuyển so với hạt nhân. Hành xử này tạo nên orbital nguyên tử, một hàm toán học đặc trưng cho xác suất một electron xuất hiện tại một điểm cụ thể khi đo vị trí của electron.[62] Chỉ có tập rời rạc bị lượng tử hóa những orbital tồn tại xung quanh hạt nhân, hoặc nếu có những dạng sóng khác thì nó sẽ nhanh chóng phân hủy thành dạng sóng đứng lượng tử ổn định hơn.[63] Các orbital có thể có cấu trúc nhiều hơn một vòng hoặc nút, và chúng khác nhau về kích thước, hình dạng và hướng.[64]

Mỗi orbital tương ứng với một mức năng lượng cụ thể của electron. Electron có thể thay đổi trạng thái của nó đến mức năng lượng cao hơn bằng hấp thụ một photon với năng lượng phù hợp để đẩy điện tử lên trạng thái năng lượng mới. Tương tự như vậy, thông qua phát xạ tự phát, một electron ở trạng thái năng lượng cao hơn có thể trở về mức năng lượng thấp bằng phát ra một photon. Những giá trị năng lượng đặc trưng này, xác định bởi hiệu giữa các mức năng lượng của từng trạng thái lượng tử, thể hiện cho dãy vạch phổ đặc trưng của từng nguyên tử.[63]
Lượng năng lượng cần để lấy đi hoặc thêm một electron vào – năng lượng liên kết electron – nhỏ hơn nhiều so với năng lượng liên kết các nucleon trong hạt nhân. Ví dụ, chỉ cần 13,6 eV để tách electron ở trạng thái năng lượng nền (trạng thái năng lượng thấp nhất) ra khỏi nguyên tử hydro,[65] so với 2,23 triệu eV để tách một hạt nhân deuteri.[66] Các nguyên tử trung hòa điện nếu chúng có số electron bằng số proton. Nguyên tử thiếu hoặc dư thừa electron gọi là ion. Những electron nằm xa hạt nhân nhất có thể bị bắt sang nguyên tử bên cạnh hoặc thuộc về cả hai nguyên tử. Theo cơ chế này, các nguyên tử có thể liên kết với nhau thành các phân tử hoặc những hợp chất hóa học khác như mạng lưới tinh thể ion hoặc liên kết cộng hóa trị.[67]
Tính chất
[sửa | sửa mã nguồn]Tính chất hạt nhân
[sửa | sửa mã nguồn]Theo định nghĩa, bất kỳ hai nguyên tử với cùng số proton trong hạt nhân thì thuộc về cùng một nguyên tố hóa học. Các nguyên tử có cùng số proton nhưng khác số neutron là những đồng vị khác nhau của cùng một nguyên tố. Ví dụ, mọi nguyên tử hydro chỉ chứa một proton, nhưng có đồng vị không chứa neutron (hydro-1, là dạng phổ biến nhất,[68] hay còn gọi là proti), chứa một neutron (deuteri), hai neutron (triti) và nhiều hơn hai neutron. Các nguyên tố đã biết lập thành một tập nguyên tử số, từ nguyên tố chứa 1 proton hydro cho đến nguyên tố chứa 118 proton oganesson.[69] Tất cả các đồng vị đã biết của nguyên tố có nguyên tử số lớn hơn 82 là đồng vị phóng xạ.[70][71]
Các nhà vật lý hạt nhân biết khoảng 339 nuclit xuất hiện trong tự nhiên trên Trái Đất,[72] trong số đó 254 (khoảng 75%) nuclit không có tính phân rã, và thường gọi là "đồng vị bền". Tuy nhiên, chỉ 90 trong số những nuclit này là ổn định đối với mọi phân rã, thậm chí ngay cả trên lý thuyết. Còn lại 164 (trong tổng số 254) thì người ta vẫn chưa quan sát thấy chúng phân rã, vì trên lý thuyết chúng có mức năng lượng hạt nhân cao. Và các nhà khoa học thường phân loại chúng một cách hình thức thuộc dạng "bền". Thêm khoảng 34 nuclit phóng xạ có nửa thời gian sống hơn 80 triệu năm, đủ lâu để có mặt từ lúc hình thành Hệ Mặt Trời. Tổng số 288 nuclit này gọi là các nuclit nguyên thủy. Cuối cùng, có thêm khoảng 51 nuclit với nửa thời gian sống ngắn mà các nhà khoa học biết chúng tồn tại trong tự nhiên, như là sản phẩm phân rã của các nuclit nguyên thủy (như radi từ urani), hoặc là những sản phẩm của các quá trình năng lượng cao trong tự nhiên trên Trái Đất, như do các tia vũ trụ bắn phá (ví dụ, cacbon-14).[73][ct 2]
Đối với 80 nguyên tố hóa học, mỗi nguyên tố có ít nhất một đồng vị bền tồn tại. Như một quy tắc, chỉ có một số nhất định đồng vị bền cho mỗi nguyên tố, trung bình khoảng 3,2 đồng vị bền trên một nguyên tố. 26 nguyên tố chỉ có duy nhất một đồng vị ổn định, trong khi nguyên tố có nhiều đồng vị bền nhất đã được xác nhận đó là thiếc với 10 đồng vị bền. Nguyên tố 43, 61, 83 và mọi nguyên tố có nguyên tử số cao hơn đều không có đồng vị bền.[74]
Tính ổn định của đồng vị bị ảnh hưởng bởi tỉ số của proton trên neutron, và cũng bởi sự có mặt của những "số thần kỳ" xác định của neutron hay proton mà xuất hiện làm đầy hoặc gần với lớp vỏ lượng tử trong mô hình cấu trúc hạt nhân. Những vỏ lượng tử này tương ứng với tập mức năng lượng trong mô hình vỏ hạt nhân; những vỏ được lấp đầy, như vỏ lượng tử của thiếc chứa đầy 50 proton, lại được coi là có tính ổn định kỳ lạ đối với nuclit (hay số thần kỳ là 50). Trong 254 nuclit bền đã biết, chỉ có bốn nuclit bền chứa đồng thời số lẻ proton và số lẻ neutron: hydro-2 (deuteri), lithi-6, boron-10 và nitơ-14. Cũng vậy, chỉ có bốn nuclit xuất hiện trong tự nhiên với đồng thời số lẻ proton và neutron có nửa thời gian sống trên một tỷ năm: kali-40, vanadium-50, lanthanum-138 và tantalum-180m. Đa số các hạt nhân có đồng thời số lẻ proton và neutron đều mất ổn định và nhanh chóng phân rã beta, bởi vì sản phẩm phân rã chứa số chẵn đồng thời proton và neutron, và do vậy liên kết chặt với nhau hơn, do hiệu ứng bắt cặp hạt nhân (theo nguyên lý loại trừ Pauli, một proton có spin lên sẽ có xu hướng bắt cặp với một proton có spin xuống, và tương tự cho neutron, điều này dẫn đến xu hướng có đồng thời số chẵn cả proton và neutron trong hạt nhân).[74]
Khối lượng
[sửa | sửa mã nguồn]Phần lớn khối lượng của nguyên tử là do đóng góp của proton và neutron trong hạt nhân của nó. Tổng những hạt này (gọi là "nucleon") trong một nguyên tử gọi là số khối. Số khối đơn giản chỉ là một số tự nhiên, có đơn vị là "nucleon." Ví dụ sử dụng số khối là "cacbon-12," có 12 nucleon (6 proton và 6 neutron).
Khối lượng thực của nguyên tử khi nó đứng yên (khối lượng bất biến, khối lượng nghỉ) thường được biểu diễn bằng đơn vị khối lượng nguyên tử (u), hay đôi khi gọi là một dalton (Da). Đơn vị này được xác định bằng một phần mười hai khối lượng nghỉ của nguyên tử tự do trung hòa điện cacbon-12, với khối lượng xấp xỉ 166×10−27 kg.[75] hydro-1, đồng vị nhẹ nhất của hydro và là nguyên tử nhẹ nhất, có khối lượng nghỉ bằng 1,007825 u.[76] Giá trị của số này gọi là nguyên tử lượng. Một nguyên tử có nguyên tử lượng xấp xỉ bằng (sai số 1%) số khối của nó nhân với đơn vị khối lượng nguyên tử. Tuy nhiên, giá trị này sẽ không bằng chính xác số khối trừ trường hợp của cacbon-12 (xem bên dưới)[77] Nguyên tử bền nặng nhất là chì-208,[70] có khối lượng là 2079766521 u.[78]
Ngay cả đối với các nguyên tử nặng nhất cũng quá nhẹ để có thể nghiên cứu trực tiếp và đơn vị khối lượng khá rườm rà, thay vào đó các nhà hóa học sử dụng đơn vị Mol. Một mol nguyên tử của bất kỳ một nguyên tố hóa học luôn có cùng số lượng nguyên tử (bằng khoảng 6022×1023). Số này được chọn sao cho nếu một nguyên tố có nguyên tử lượng là 1 u, thì 1 mol nguyên tử nguyên tố này có khối lượng xấp xỉ 1 gram. Do định nghĩa của đơn vị khối lượng nguyên tử, mỗi nguyên tử cacbon-12 có nguyên tử khối chính xác bằng 12 u, do vậy 1 mol nguyên tử cacbon-12 có khối lượng chính xác bằng 0,012 kg.[75]
Hình dạng và kích thước
[sửa | sửa mã nguồn]Nguyên tử không có bề mặt định rõ, do vậy kích thước của nó thường được xác định hình thức bằng thuật ngữ bán kính nguyên tử. Đại lượng này đo khoảng cách mở rộng đám mây electron tính từ hạt nhân. Tuy nhiên, cách giả sử này không chỉ đúng cho nguyên tử có dạng hình cầu, mà còn đúng cho nguyên tử cô lập trong chân không. Bán kính nguyên tử có thể suy ra từ khoảng cách giữa hai hạt nhân khi hai nguyên tử kết hợp lại theo liên kết hóa học. Bán kính thay đổi phụ thuộc vị trí của nguyên tử trên bảng tuần hoàn, loại liên kết hóa học, số nguyên tử hay ion lân cận với nó (số tọa độ) và tính chất cơ học lượng tử của nó spin.[79] Trên bảng tuần hoàn nguyên tố hóa học, theo tính toán lý thuyết, kích thước nguyên tử có xu hướng tăng lên khi đi theo cột từ trên xuống, nhưng giảm khi đi theo hàng từ trái sang phải và dữ liệu thực nghiệm đo được khá phù hợp với xu hướng này.[80] Hệ quả là nguyên tử có bán kính nhỏ nhất là 32 pm, trong khi nguyên tử lớn nhất là caesi với bán kính 225 pm.[81]
Khi chịu tác động của trường ngoài, như điện trường và từ trường, hình dạng của nguyên tử có thể bị bẻ lệch khỏi hình cầu. Sự lệch này phụ thuộc vào cường độ của trường và kiểu orbital của lớp vỏ electron ngoài cùng, như được chỉ ra bởi lý thuyết nhóm. Hình cầu biến dạng có thể xuất hiện trong cấu trúc tinh thể ở đây khi chịu điện trường mẫu tinh thể có xuất hiện những đối xứng bậc thấp trong dàn tinh thể.[82] Gần đây các nhà tinh thể học chỉ ra sự biến dạng lớn thành ellipsoid xuất hiện ở ion lưu huỳnh trong tinh thể pyrit.[83]


Nguyên tử có kích thước nhỏ hơn hàng nghìn lần bước sóng ánh sáng khả kiến (400–700 nm) do vậy chúng ta không thể quan sát nguyên tử bằng kính hiển vi quang học. Tuy nhiên, có thể quan sát từng nguyên tử bằng thiết bị kính hiển vi quét xuyên hầm. Để hình dung kích thước rất nhỏ của nguyên tử, đường kính của tóc người bình thường bằng khoảng 1 triệu lần đường kính nguyên tử cacbon.[84] Một giọt nước chứa khoảng (2×1021) nguyên tử oxy, và gấp hai lần số nguyên tử hydro.[85] Một cara kim cương với khối lượng 2×10−4 kg chứa khoảng (1022) nguyên tử cacbon.[ct 3] Nếu một quả táo phóng to bằng đường kính Trái Đất, thì một nguyên tử trong quả táo có đường kính xấp xỉ kích cỡ quả táo ban đầu.[86]
Phân rã phóng xạ
[sửa | sửa mã nguồn]Mỗi nguyên tố có một hay nhiều đồng vị mà hạt nhân không bền sẽ tiến tới phân rã phóng xạ, và hạt nhân phát ra hạt nhân khác hoặc bức xạ điện từ. Hiện tượng phóng xạ xảy ra khi bán kính của hạt nhân đủ lớn so với bán kính ảnh hưởng của tương tác mạnh, với phạm vi tác động khoảng 1 fm.[87]
Những phản ứng phân rã phóng xạ hay gặp nhất là:[88][89]
- Phân rã alpha là phản ứng trong đó hạt nhân phát ra hạt alpha, hạt nhân của heli chứa hai proton và hai neutron. Hạt sản phẩm là những nguyên tố mới với số nguyên tử thấp hơn.
- Phân rã beta (và bắt giữ electron) bị kiểm soát bởi tương tác yếu, và kết quả là một neutron biến đổi thành một proton, hoặc một proton thành một neutron. Kiểu đầu tiên đi kèm với sự phát ra một electron và một phản neutrino electron, trong khi kiểu thứ hai phát ra một positron và một neutrino electron. Hạt electron hoặc positron phát ra vì lý do lịch sử mà các nhà vật lý gọi là những hạt beta. Phân rã beta làm tăng hoặc giảm số nguyên tử của hạt nhân 1 đơn vị. Một phản ứng tương tự với phân ra beta của hạt positron trong hạt nhân giàu proton đó là phản ứng bắt electron của hạt nhân, quá trình này thậm chí còn phổ biến hơn phản ứng phát ra positron do nó đòi hỏi ít năng lượng hơn. Trong phản ứng này electron bị hấp thụ bởi hạt nhân hơn là phát positron. Một hạt neutrino vẫn phát ra trong phản ứng và một proton biến thành một neutron.
- Phóng xạ tia gamma làm thay đổi mức năng lượng của hạt nhân về trạng thái năng lượng thấp hơn, kết quả là phát ra photon gamma. Phản ứng này có thể xuất hiện sau phân rã alpha hoặc beta từ phân rã phóng xạ.
Một loại phân rã hiếm nữa là sản phẩm phân rã bao gồm những neutron hoặc proton hoặc đám nucleon từ một hạt nhân, hoặc có nhiều hơn một hạt beta bị bắn ra, hoặc sản phẩm (thông qua biến đổi nội bộ hạt nhân gốc) là những electron năng lượng cao mà không phải là chùm tia beta, hay những photon năng lượng cao không phải là tia gamma. Một vài hạt nhân nổ thành hai hoặc nhiều hạt nhân không cố định đi kèm với một số neutron, trong phân rã tự phát của phản ứng phân hạch hạt nhân.
Mỗi đồng vị phóng xạ có chu kỳ phân rã đặc trưng — hay nửa thời gian sống — xác định bởi lượng thời gian cần thiết cho một nửa mẫu hạt phân rã. Đây là tiến trình phân rã hàm mũ và giảm dần lượng đồng vị còn lại một nửa sau mỗi chu kỳ phân rã. Do đó sau chu kỳ phân rã thứ hai số hạt đồng vị còn lại chỉ là 25% so với ban đầu, và cứ như thế.[87]
Mômen từ
[sửa | sửa mã nguồn]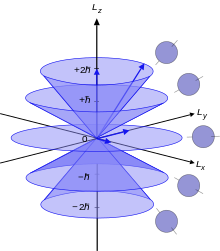
Các hạt cơ bản có một tính chất cơ học lượng tử nội tại gọi là spin. Tính chất này tương tự như động lượng góc của một vật quay quanh khối tâm của nó, mặc dù nói một cách sơ lược những hạt cơ bản được cho là những hạt điểm và không thể hiện tính tự quay quanh trục nào cả. Spin lượng tử hay mômen từ nội tại có đơn vị đo bằng hằng số Planck thu gọn (ħ), với electron, proton và neutron chúng chỉ có hai giá trị spin ½ ħ, hoặc "spin -½". Trong nguyên tử, các electron bao quanh hạt nhân có mômen động lượng orbital cùng với đặc tính spin, trong khi hạt nhân có mômen động lượng chính nó do spin của hạt nhân.[90]
Từ trường sinh ra bởi nguyên tử—mômen từ— được xác định bởi nhiều giá trị mô men động lượng, giống như một vật tích điện chuyển động trong điện từ học cổ điển sinh ra từ trường. Tuy nhiên, đóng góp chủ yếu đến từ spin. Do bản chất các electron tuân theo nguyên lý loại trừ Pauli, hai electron không thể có cùng một trạng thái lượng tử trong một vùng ở cùng thời gian (không có cùng 4 số lượng tử) và quy tắc Hund về quy trình phân bố electron trong orbital. Các electron liên kết tạo cặp với nhau trong orbital, với một electron có trạng thái spin lên và electron kia có trạng thái spin xuống. Do vậy trong một cặp, spin lượng tử bị triệt tiêu, dẫn đến tổng mômen lưỡng cực từ bằng 0 trong một số nguyên tử có số chẵn electron với mỗi orbital đã lấp đầy bởi những cặp electron.[91]
Trong các nguyên tố sắt từ như sắt, niken, chúng có một số electron chưa bắt cặp trong orbital và vì vậy có mômen từ nguyên tử. orbital của các nguyên tử lân cận phủ lên nhau và xuất hiện một trạng thái năng lượng thấp hơn khi spin của các electron chưa bắt cặp đồng loạt hướng theo nhau, một quá trình gọi là tương tác trao đổi. Khi mômen từ của các nguyên tử sắt từ sắp hàng, vật liệu sẽ sinh ra một từ trường vĩ mô đo được. Nguyên tử của vật liệu thuận từ có mômen từ sắp xếp ngẫu nhiên không theo một hướng, nhưng khi có từ trường ngoài thì các mômen từ hưởng ứng theo hướng của từ trường ngoài và có một từ trường vĩ mô nhỏ ở vật liệu thuận từ.[91][92]
Hạt nhân nguyên tử cũng có spin. Thông thường các hạt nhân có spin định hướng theo những hướng ngẫu nhiên trong cân bằng nhiệt động. Tuy nhiên, đối với một số nguyên tố (như xenon-129) hạt nhân của nó có thể bị phân cực spin theo số lượng lớn của trạng thái spin hạt nhân do vậy chúng có thể sắp hàng theo một hướng— hay hiện tượng siêu phân cực. Spin hạt nhân có một ứng dụng quan trọng trong y học đó là chụp ảnh cộng hưởng từ hạt nhân.[93][94]
Mức năng lượng
[sửa | sửa mã nguồn]
Các nhà vật lý quy ước thế năng của một electron trong nguyên tử có giá trị âm, và phụ thuộc vào vị trí của nó trong nguyên tử. Nó có giá trị cực tiểu khi nằm ở gần hạt nhân nhất và quy ước bằng 0 khi nó nằm xa vô cùng so với hạt nhân, hay thế năng của nó tỉ lệ nghịch với khoảng cách. Trong mô hình cơ học lượng tử, một electron liên kết chỉ có thể chiếm những trạng thái lượng tử xung quanh hạt nhân, và mỗi trạng thái tương ứng với một mức năng lượng xác định; xem phương trình Schrödinger độc lập thời gian về cách giải thích lý thuyết. Mức năng lượng có thể đo bằng lượng năng lượng cần thiết để bứt electron tại trạng thái đó ra xa vô cùng, và có đơn vị electronvolt (eV). Trạng thái năng lượng thấp nhất của electron liên kết gọi là trạng thái năng lượng nền[95] và khi một electron chuyển dịch sang mức năng lượng cao hơn thì nó ở vào trạng thái kích thích.[96] Năng lượng của electron tăng lên khi số lượng tử chính n tăng bởi vì khoảng cách trung bình đến hạt nhân tăng. Sự phụ thuộc năng lượng vào số lượng tử xung lượng ℓ không phải là do thế năng tĩnh điện với hạt nhân mà là bởi tương tác giữa các electron.
Khi một electron chuyển dịch giữa hai trạng thái năng lượng, nó phải hấp thụ hoặc phát ra một photon có năng lượng bằng hiệu giữa hai trạng thái năng lượng này.[97] Năng lượng của một photon tỷ lệ với tần số của nó, do đó những mức năng lượng xác định này hiện lên thành những dải phân biệt trong phổ điện từ.[98] Mỗi nguyên tố có một phổ đặc trưng phụ thuộc vào điện tích hạt nhân, cấu hình electron, tương tác điện từ giữa các electron và bởi những nhân tố khác.[99]

Khi ánh sáng với phổ năng lượng liên tục truyền qua chất khí hay plasma, một số nguyên tử hấp thụ photon, khiến cho các electron thay đổi mức năng lượng của nó. Những electron kích thích này vẫn liên kết với nguyên tử của nó và tự phát phóng thích năng lượng qua phát ra photon theo hướng ngẫu nhiên, và trở lại trạng thái năng lượng thấp hơn. Do vậy nguyên tử thể hiện như một máy lọc tạo ra một dãy các vạch tối trong phổ năng lượng phát ra. (Một người quan sát nguyên tử khi chùm sáng chiếu qua chúng sẽ thấy khi lọc bỏ phổ liên tục thu được dãy phổ phát xạ đặc trưng của nguyên tử.) Đo lường phổ về cường độ và độ rộng của các vạch phổ nguyên tử cho phép các nhà khoa học xác định được thành phần và tính chất vật lý của chất cần nghiên cứu.[100]
Khi nghiên cứu kĩ hơn phổ nguyên tử các nhà vật lý nhận thấy có sự tách vạch trong cấu trúc tế vi. Sự xuất hiện này là do hiệu ứng spin-quỹ đạo tương đối tính, khi tính đến ảnh hưởng giữa chuyển động của electron lớp ngoài cùng với spin của nó.[101] Khi nguyên tử đặt trong từ trường ngoài, các vạch phổ của nó bị tách thành ba hoặc nhiều vạch; hay hiệu ứng Zeeman. Hiệu ứng này là do tương tác của từ trường ngoài với mômen từ của nguyên tử và của electron. Một số nguyên tử có nhiều cấu hình electron với cùng một mức năng lượng, do đó vạch phổ thu được là giống nhau cho những cấu hình này. Khi nguyên tử tương tác với từ trường làm dịch chuyển những cấu hình electron đến một mức năng lượng hơi khác, làm cho xuất hiện nhiều vạch phổ trên quang phổ thu được.[102] Sự có mặt của một điện trường ngoài cũng làm tách và dịch chuyển vạch phổ và thay đổi đáng kể mức năng lượng của electron, hay hiệu ứng Stark.[103]
Nếu electron liên kết trong trạng thái kích thích, một photon tương tác với năng lượng riêng có thể gây ra hiệu ứng phát xạ kích thích cho một photon với năng lượng phù hợp với mức kích thích. Để điều này xảy ra, electron phải trở về trạng thái năng lượng thấp hơn mà có hiệu năng lượng giữa hai trạng thái chuyển dịch bằng với năng lượng của photon tương tác. Photon phát ra và photon tương tác di chuyển song song và có cùng pha với nhau, phản xạ qua lại giữa hai gương. Khi đó, phần sóng của hai photon được đồng bộ hóa. Tính chất vật lý này được ứng dụng để chế tạo các loại laser, một chùm sóng điện từ kết hợp với tần số đồng bộ.[104]
Hóa trị và liên kết hóa học
[sửa | sửa mã nguồn]Lớp vỏ electron ngoài cùng của nguyên tử cô lập trong trạng thái chưa kết hợp gọi là vỏ hóa trị, và các electron trong lớp vỏ này gọi là electron hóa trị. Số các electron hóa trị xác định lên tính chất liên kết hóa học giữa các nguyên tử với nhau. Nguyên tử có xu hướng phản ứng với nhau theo cách lấp đầy (hoặc làm trống) các vỏ hóa trị ngoài cùng của chúng.[105] Ví dụ, sự truyền đổi một electron giữa các nguyên tử là một cách xấp xỉ tốt cho liên kết hình thành giữa một nguyên tử cần thêm một electron là đầy lớp vỏ hóa trị với một nguyên tử khi bớt một electron nó sẽ đầy lớp vỏ, cách liên kết này xuất hiện trong hợp chất natri chloride và những muối ion khác. Tuy nhiên, nhiều nguyên tố có nhiều số hóa trị, và có xu hướng chia sẻ nhiều electron khác nhau trong những hợp chất khác nhau. Như thế, các liên kết hóa học giữa những nguyên tố hình thành theo kiểu chia sẻ nhiều electron hơn là chỉ truyền đổi một electron. Ví dụ này bao gồm nguyên tố cacbon và các hợp chất hữu cơ.[106]
Tính chất hóa học của các nguyên tố thể hiện tính tuần hoàn khi sắp xếp trên bảng tuần hoàn, và các nguyên tố với cùng số electron hóa trị tạo thành một nhóm trong cùng một cột của bảng. (Hàng ngang tương ứng với sự lấp đầy lớp vỏ electron.) Các nguyên tố ở phía ngoài cùng bên phải của bảng có lớp vỏ hóa trị đã được lấp đầy electron, khiến cho những nguyên tố này rất thụ động trong các phản ứng hóa học, hay còn gọi là khí hiếm.[107][108]
Trạng thái
[sửa | sửa mã nguồn]
Các nguyên tử tham gia cấu thành lên những trạng thái vật chất khác nhau phụ thuộc vào những điều kiện vật lý, như mật độ, nhiệt độ và áp suất. Khi những điều kiện này thay đổi đến điều kiện giới hạn, xảy ra sự chuyển pha vật chất giữa các pha rắn, lỏng, khí và plasma. [109] Trong một trạng thái, vật liệu cũng thể hiện những dạng thù hình khác nhau. Ví dụ như đối với cacbon rắn, nó có thể hiện như graphen, graphit hay kim cương.[110] Dạng thù hình trong chất khí cũng tồn tại, như dioxy và ozone.
Quan sát và thăm dò
[sửa | sửa mã nguồn]
Các nhà khoa học sử dụng kính hiển vi quét chui hầm là thiết bị quan sát bề mặt vật liệu ở cấp nguyên tử. Nguyên lý hoạt động của nó dựa trên hiệu ứng đường hầm lượng tử, hiệu ứng cho phép các hạt đi qua rào cản là giếng thế mà về mặt trực giác vĩ mô là không thể. Các electron chui hầm qua chân không giữa hai điện cực kim loại đồng phẳng, trên mỗi phía có một nguyên tử hấp thụ electron, dẫn đến xuất hiện mật độ dòng điện mà có thể đo được. Khi đầu dò được quét trên bề mặt mẫu, sẽ xuất hiện các điện tử di chuyển từ bề mặt mẫu sang mũi dò do hiệu ứng chui hầm lượng tử và việc ghi lại dòng chui hầm (do một hiệu điện thế đặt giữa mũi dò và mẫu) này sẽ cho các thông tin về cấu trúc bề mặt.[111][112]
Khi nguyên tử bị mất một vài electron nó trở thành ion. Khi là hạt điện tích quỹ đạo của nó bị lệch đi trong từ trường. Đo được bán kính độ lệch quỹ đạo của ion cho phép chúng ta xác định được khối lượng của nguyên tử. Thiết bị phổ khối kế dựa trên nguyên lý này để đo tỉ số khối lượng trên điện tích của các ion. Nếu một chứa nhiều ion, phổ khối có thể xác định được tỉ lệ của mỗi đồng vị trong mẫu bằng cách đo cường độ của nhiều chùm ion khác nhau. Kỹ thuật làm bay hơi nguyên tử bao gồm "phổ kế phát xạ cặp nguyên tử plasma cảm ứng" và "phổ kế khối lượng cặp plasma cảm ứng", cả hai kỹ thuật sử dụng plasma làm bay hơi mẫu để phân tích.[113]
Một phương pháp hay dùng nữa là phổ tổn hao năng lượng điện tử, dựa trên việc ghi và phân tích phần năng lượng bị mất mát của chùm electron trong kính hiển vi điện tử truyền qua do tán xạ không đàn hồi khi truyền qua mẫu vật rắn. Phương pháp thăm dò nguyên tử (atom probe) có độ phân giải dưới nanômét và thu được ảnh 3-D cũng như xác định được đặc tính hóa học của từng nguyên tử thông qua phổ khối thời gian truyền.[114]
Phổ của trạng thái nguyên tử kích thích được dùng để phân tích thành phần nguyên tử trong các sao ở xa. Các nhà thiên văn có thể tách những bước sóng điện từ đặc trưng trong ánh sáng phát ra từ ngôi sao và liên hệ nó với sự dịch chuyển lượng tử trong nguyên tử khí tự do. Những màu này (bước sóng) có thể được sao chép bằng cách sử dụng đèn phóng điện qua khí (gas-discharge lamp) chứa cùng nguyên tố trên ngôi sao.[115] Đặc biệt nguyên tử Heli đã được phát hiện theo cách này khi nghiên cứu phổ Mặt Trời sớm 23 năm trước khi nó được phát hiện có tồn tại trên Trái Đất.[116]
Nguồn gốc và trạng thái hiện tại
[sửa | sửa mã nguồn]Nguyên tử chiếm khoảng 4,9% tổng mật độ năng lượng trong Vũ trụ quan sát được[117] (còn lại là vật chất tối và năng lượng tối), với mật độ trung bình khoảng 0,25 nguyên tử/m³.[118] Trong một thiên hà như Ngân Hà, nguyên tử có độ tập trung cao hơn, với mật độ vật chất bên trong môi trường liên sao (ISM) từ 105 đến 109 nguyên tử/m³.[119] Mặt Trời nằm trong Bong bóng địa phương, một vùng tập trung khí ion hóa cao, do vậy mật độ ở môi trường lân cận hệ Mặt Trời trung bình vào khoảng 103 nguyên tử/m³.[120] Các ngôi sao hình thành từ những đám mây đậm đặc trong ISM, và quá trình tiến hóa của sao dần dần làm giàu môi trường trong ISM với các nguyên tố nặng hơn hydro và heli. Có tới 95% nguyên tử trong Ngân Hà tập trung bên trong các ngôi sao và tổng khối lượng nguyên tử chiếm khoảng 10% khối lượng toàn thiên hà.[121] (phần khối lượng còn lại đa số là vật chất tối.)[122]
Sự hình thành
[sửa | sửa mã nguồn]Electron tồn tại trong Vũ trụ từ giai đoạn sơ khai sau Vụ nổ lớn. Hạt nhân nguyên tử hình thành trong các phản ứng tổng hợp hạt nhân. Quá trình tổng hợp hạt nhân sau Vụ nổ lớn tạo ra phần lớn heli, lithi, và deuteri trong Vũ trụ, và có lẽ là beryli và bo.[123][124][125]
Sự tồn tại khắp nơi và tính ổn định của nguyên tử dựa trên năng lượng liên kết của nó, có nghĩa là nguyên tử có năng lượng thấp hơn so với một hệ không liên kết gồm hạt nhân và các electron. Khi nhiệt độ cao hơn năng lượng ion hóa nguyên tử, vật chất tồn tại ở trạng thái plasma – chất khí chứa ion điện tích dương (hoặc thậm chí cả hạt nhân trần trụi) và electron. Khi nhiệt độ giảm xuống dưới mức năng lượng ion hóa, các nguyên tử bắt đầu hình thành theo các định luật của vật lý thống kê. Nguyên tử (khi đã bắt các electron) trở lên vượt trội so với các hạt tích điện sau 380.000 năm từ Big Bang— một kỷ nguyên gọi là "tái kết hợp", khi Vũ trụ giãn nở ra và lạnh đi cho phép các electron gắn kết được với hạt nhân.[126]
Do Vụ nổ lớn không sinh ra cacbon hoặc nguyên tử nặng hơn, hạt nhân nguyên tử được sản sinh trong lòng các ngôi sao thông qua phản ứng tổng hợp hạt nhân để tạo ra nhiều nguyên tố heli hơn, và (thông qua quá trình bộ ba heli) sản sinh ra các nguyên tố cacbon cho tới sắt;[127] xem thêm tổng hợp hạt nhân sao.
Những loại đồng vị như lithi-6, cũng như một số đồng vị berylilli và bo sản sinh trong không gian thông qua phản ứng bắn phá của tia vũ trụ.[128] Khi chùm tia proton năng lượng cao va đập vào hạt nhân nguyên tử trong khí quyển Trái Đất, khiến cho một lượng lớn số hạt nhân nhẹ sinh ra.
Những nguyên tố nặng hơn sắt hình thành trong vụ nổ siêu tân tinh thông qua quá trình-r (r-process) và trong các sao nhánh tiệm cận khổng lồ (AGB stars) thông qua quá trình-s (s-process), cả hai quá trình có sự bắt neutron của hạt nhân nguyên tử.[129]
Trái Đất
[sửa | sửa mã nguồn]
Hầu hết các nguyên tử cấu tạo nên Trái Đất và những thứ tồn tại trên nó đã có mặt trong những tinh vân suy sụp hấp dẫn từ đám mây phân tử để hình thành lên Hệ Mặt Trời. Một số hạt nhân còn lại là sản phẩm của quá trình phân rã, và khi đo được tỷ lệ có mặt của chúng các nhà khoa học có thể xác định được tuổi của Trái Đất thông qua định tuổi bằng đồng vị phóng xạ.[130][131] Hầu hết heli trong lớp vỏ Trái Đất (khoảng 99% khí heli xuất hiện trong các giếng khai thác khí đốt, và một lượng nhỏ heli-3) là sản phẩm của phản ứng phân rã alpha.[132]
Một vài dấu vết của một số đồng vị nguyên tử trên Trái Đất không có mặt lúc hình thành hệ Mặt Trời (hay không phải là "nguyên thủy"), hay là sản phẩm của quá trình phân rã. Cacbon-14 liên tục được sinh ra từ tia vũ trụ trong khí quyển.[133] Một số nguyên tử trên Trái Đất sinh ra từ các máy gia tốc hay trong lò phản ứng hạt nhân hoặc các vụ thử nghiệm vũ khí nguyên tử.[134][135] Trong các nguyên tố siêu urani—với số nguyên tử lớn hơn 92—chỉ có plutoni và neptuni xuất hiện trong tự nhiên trên Trái Đất.[136][137] Các nguyên tố siêu urani có chu kỳ phân rã phóng xạ ngắn hơn tuổi của Trái Đất [138] và do vậy nếu chúng hình thành nguyên thủy thì cũng đã bị phân rã từ lâu, ngoại trừ có một ít plutoni-244 xuất hiện trong bụi vũ trụ.[139] Nguyên tố plutoni và neptuni có trong tự nhiên chủ yếu là sản phẩm của urani bắt neutron và thường thấy ở các quặng urani.[140]
Trái Đất chứa xấp xỉ 133×1050 nguyên tử.[141] Mặc dù có dạng nguyên tử tồn tại độc lập như các khí hiếm tồn tại ít, như argon, neon, và heli, 99% khí quyển chứa chủ yếu các nguyên tử dạng kết hợp như phân tử, bao gồm cacbon dioxide CO2 và phân tử hai nguyên tử như oxy O2 và nitơ N2. Tại bề mặt Trái Đất, lượng khổng lồ các nguyên tử kết hợp theo nhiều dạng, bao gồm nước H2O, muối, silicat và các oxide. Nguyên tử cũng kết hợp lại thành vật liệu không chứa phân tử rời rạc, bao gồm tinh thể và chất lỏng hoặc kim loại rắn.[142][143] Dạng vật chất nguyên tử này tạo nên mạng lưới được sắp xếp thiếu đi kiểu trật tự gián đoạn loại đặc biệt quy mô nhỏ thường gặp ở dạng vật chất phân tử.[144]
Các dạng hiếm và trên lý thuyết
[sửa | sửa mã nguồn]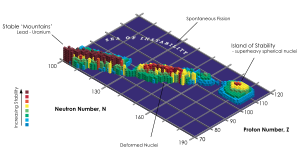
Nguyên tố siêu nặng
[sửa | sửa mã nguồn]Các đồng vị với số nguyên tử lớn hơn của chì (82) có tính phóng xạ, các nhà vật lý đã đề xuất về sự tồn tại của "đảo bền" cho những nguyên tố có số nguyên tử lớn hơn 103. Những nguyên tố siêu nặng này có hạt nhân tương đối ổn định trong quá trình phân rã.[145] Ứng cử viên cho nguyên tử siêu nặng ổn định đó là unbihexium, có 126 proton và 184 neutron.[146]
Vật chất ngoại lai
[sửa | sửa mã nguồn]Mỗi hạt vật chất đều có dạng tương ứng trên lý thuyết đó là hạt phản vật chất với điện tích trái dấu. Hay hạt positron điện tích dương là phản hạt của electron và phản proton điện tích âm là phản hạt của proton. Khi vật chất và phản vật chất tương ứng gặp nhau chúng lập tức bị hủy thành các tia gamma. Bởi vì lý do này, cùng với sự mất cân bằng giữa lượng vật chất và phản vật chất trong vũ trụ, phản vật chất rất hiếm thấy trong vũ trụ. (Mặc dù nguyên nhân của sự mất cân bằng trên quy mô Vũ trụ chưa được hiểu đầy đủ, một số lý thuyết đã đề xuất ra về sự vi phạm đối xứng CPT trong thời điểm của Vụ nổ lớn.) Và hiện nay chưa có nguyên tử phản vật chất nào tìm thấy tồn tại trong tự nhiên.[147][148] Trong phòng thí nghiệm, năm 1996, trung tâm nghiên cứu hạt hạ nguyên tử CERN ở Genève đã lần đầu tiên tạo ra được phản hydro.[149][150]
Các nhà vật lý cũng tạo ra được những nguyên tử ngoại lai khác bằng cách thay hạt proton, neutron hay electron bằng hạt khác có cùng điện tích. Ví dụ, trong nguyên tử hydro hạt electron được thay thế bằng lepton nặng hơn là muon, tạo ra nguyên tử muonic. Nguyên tử lạ là một trong những mẫu để các nhà vật lý kiểm chứng các tiên đoán cơ bản của vật lý.[151][152][153]
Xem thêm
[sửa | sửa mã nguồn]Chú thích
[sửa | sửa mã nguồn]- ^ Trong trường hợp của hydro-1, với 1 electron và 1 proton, khối lượng proton bằng , hay chiếm tới 99,946% tổng khối lượng nguyên tử. Tất cả những nuclit khác (đồng vị của hydro và tất cả nguyên tố khác) có nhiều nucleon hơn electron, do vậy tỉ số khối lượng của hạt nhân gần bằng với 100% đối với mọi loại nguyên tử, nhiều hơn so với hydro-1.
- ^ Bảng dữ liệu cập nhật xem tại Interactive Chart of Nuclides (Brookhaven National Laboratory) Lưu trữ 2020-07-25 tại Wayback Machine.
- ^ Một cara bằng 200 milligram. Theo định nghĩa, cacbon-12 có khối lượng 0,012 kg trên mol. Hằng số Avogadro xác định 6×1023 nguyên tử trên mol.
Tham khảo
[sửa | sửa mã nguồn]- ^ Leigh, G. J. biên tập (1990). International Union of Pure and Applied Chemistry, Commission on the Nomenclature of Inorganic Chemistry, Nomenclature of Organic Chemistry – Recommendations 1990. Oxford: Blackwell Scientific Publications. tr. 35. ISBN 0-08-022369-9.
An atom is the smallest unit quantity of an element that is capable of existence whether alone or in chemical combination with other atoms of the same or other elements.
- ^ “Radioactive Decays”. Stanford Linear Accelerator Center. ngày 15 tháng 6 năm 2009. Bản gốc lưu trữ ngày 7 tháng 6 năm 2009. Truy cập ngày 4 tháng 7 năm 2009.
- ^ Liddell, Henry George; Scott, Robert. “A Greek-English Lexicon”. Perseus Digital Library.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Liddell, Henry George; Scott, Robert. “ἄτομος”. A Greek-English Lexicon. Perseus Digital Library. Truy cập ngày 21 tháng 6 năm 2010.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Haubold, Hans; Mathai, A.M. (1998). “Microcosmos: From Leucippus to Yukawa”. Structure of the Universe. Bản gốc lưu trữ ngày 5 tháng 5 năm 2009. Truy cập ngày 17 tháng 1 năm 2008.
- ^ Harrison 2003, tr. 123–139.
- ^ Leon M. Lederman and Dick Teresi (1993). The God Particle: If the Universe is the Answer, What is the Question?. Boston: Houghton Mifflin Company. ISBN 0-618-71168-6. Lederman đã đưa ra một thảo luận rất hay về vấn đề này.
- ^ a b Ponomarev 1993, tr. 14–15.
- ^ McEvilley 2002, tr. 317.
- ^ King 1999, tr. 105–107.
- ^ Moran 2005, tr. 146.
- ^ a b Levere 2001, tr. 7.
- ^ Pratt, Vernon (ngày 28 tháng 9 năm 2007). “The Mechanical Philosophy”. Reason, nature and the human being in the West. Bản gốc lưu trữ ngày 11 tháng 6 năm 2008. Truy cập ngày 28 tháng 6 năm 2009.
- ^ Siegfried 2002, tr. 42–55.
- ^ Kemerling, Garth (ngày 8 tháng 8 năm 2002). “Corpuscularianism”. Philosophical Dictionary. Truy cập ngày 17 tháng 6 năm 2009.
- ^ “Lavoisier's Elements of Chemistry”. Elements and Atoms. Le Moyne College, Department of Chemistry. Truy cập ngày 18 tháng 12 năm 2007.
- ^ Wurtz 1881, tr. 1–2.
- ^ Dalton 1808.
- ^ Roscoe 1895, tr. 129.
- ^ Loschmidt, J. (1865). “Zur Grösse der Luftmoleküle”. Sitzungsberylichte der kaiserlichen Akademie der Wissenschaften Wien. 52 (2): 395–413. Bản tiếng Anh: J. Loschmidt (William Porterfield và Walter Kruse chuyển ngữ), "On the size of the air molecules," Journal of Chemical Education, vol. 72, no. 10, tr. 870-875 (Tháng 10, 1995).
- ^ Einstein, Albert (1905). “Über die von der molekularkinetischen Theorie der Wärme geforderte Bewegung von in ruhenden Flüssigkeiten suspendierten Teilchen” (PDF). Annalen der Physik (bằng tiếng Đức). 322 (8): 549–560. Bibcode:1905AnP...322..549E. doi:10.1002/andp.19053220806. ISSN 0003-3804. Bản gốc (PDF) lưu trữ ngày 18 tháng 7 năm 2007. Truy cập ngày 4 tháng 2 năm 2007.
- ^ Mazo 2002, tr. 1–7.
- ^ Y.K. Lee & Hoon, K. (1995). “Brownian Motion”. Imperial College. Bản gốc lưu trữ ngày 18 tháng 12 năm 2007. Truy cập ngày 18 tháng 12 năm 2007.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ Patterson, G. (2007). “Jean Perrin and the triumph of the atomic doctrine”. Endeavour (journal). 31 (2): 50–53. doi:10.1016/j.endeavour.2007.05.003. PMID 17602746.
- ^ “Periodic Table of the Elements”. The International Union of Pure and Applied Chemistry. ngày 1 tháng 11 năm 2007. Lưu trữ bản gốc ngày 25 tháng 4 năm 2010. Truy cập ngày 14 tháng 5 năm 2010.
- ^ Scerri 2007, tr. 10–17.
- ^ “J.J. Thomson”. Nobel Foundation. 1906. Truy cập ngày 20 tháng 12 năm 2007.
- ^ Rutherford, E. (1911). “The Scattering of α and β Particles by Matter and the Structure of the Atom” (PDF). Philosophical Magazine. 21 (125): 669–88. doi:10.1080/14786440508637080.[liên kết hỏng]
- ^ “Frederick Soddy, The Nobel Prize in Chemistry 1921”. Nobel Foundation. Truy cập ngày 18 tháng 1 năm 2008.
- ^ Thomson, Joseph John (1913). “Rays of positive electricity”. Proceedings of the Royal Society. A. 89 (607): 1–20. Bibcode:1913RSPSA..89....1T. doi:10.1098/rspa.1913.0057.
- ^ Stern, David P. (ngày 16 tháng 5 năm 2005). “The Atomic Nucleus and Bohr's Early Model of the Atom”. NASA/Goddard Space Flight Center. Bản gốc lưu trữ ngày 20 tháng 8 năm 2007. Truy cập ngày 20 tháng 12 năm 2007.
- ^ Bohr, Niels (ngày 11 tháng 12 năm 1922). “Niels Bohr, The Nobel Prize in Physics 1922, Nobel Lecture”. Nobel Foundation. Truy cập ngày 16 tháng 2 năm 2008.
- ^ Pais 1986, tr. 228–230.
- ^ Lewis, Gilbert N. (1916). “The Atom and the Molecule”. Journal of the American Chemical Society. 38 (4): 762–786. doi:10.1021/ja02261a002.
- ^ Scerri 2007, tr. 205–226.
- ^ Langmuir, Irving (1919). “The Arrangement of Electrons in Atoms and Molecules”. Journal of the American Chemical Society. 41 (6): 868–934. doi:10.1021/ja02227a002.
- ^ Marlan O. Scully;Lamb, Willis E.; Barut, Asim (1987). “On the theory of the Stern-Gerlach apparatus”. Foundations of Physics. 17 (6): 575–583. Bibcode:1987FoPh...17..575S. doi:10.1007/BF01882788.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ Brown, Kevin (2007). “The Hydrogen Atom”. MathPages. Truy cập ngày 21 tháng 12 năm 2007.
- ^ Harrison, David M. (2000). “The Development of Quantum Mechanics”. University of Toronto. Bản gốc lưu trữ ngày 25 tháng 12 năm 2007. Truy cập ngày 21 tháng 12 năm 2007.
- ^ Aston, Francis W. (1920). “The constitution of atmospheric neon”. Philosophical Magazine. 39 (6): 449–55. doi:10.1080/14786440408636058.
- ^ Chadwick, James (ngày 12 tháng 12 năm 1935). “Nobel Lecture: The Neutron and Its Properties”. Nobel Foundation. Truy cập ngày 21 tháng 12 năm 2007.
- ^ “Otto Hahn, Lise Meitner and Fritz Strassmann”. Chemical Achievers: The Human Face of the Chemical Sciences. Chemical Heritage Foundation. Bản gốc lưu trữ ngày 24 tháng 10 năm 2009. Truy cập ngày 15 tháng 9 năm 2009.
- ^ Meitner, Lise; Frisch, Otto Robert (1939). “Disintegration of uranium by neutrons: a new type of nuclear reaction”. Nature (journal). 143 (3615): 239. Bibcode:1939Natur.143..239M. doi:10.1038/143239a0.
- ^ Schroeder, M. “Lise Meitner – Zur 125. Wiederkehr Ihres Geburtstages” (bằng tiếng Đức). Bản gốc lưu trữ ngày 19 tháng 7 năm 2011. Truy cập ngày 4 tháng 6 năm 2009.
- ^ Crawford, E.; Sime, Ruth Lewin; Walker, Mark (1997). “A Nobel tale of postwar injustice”. Physics Today. 50 (9): 26–32. Bibcode:1997PhT....50i..26C. doi:10.1063/1.881933. Bản gốc lưu trữ ngày 7 tháng 3 năm 2012. Truy cập ngày 3 tháng 4 năm 2013.
- ^ Kullander, Sven (ngày 28 tháng 8 năm 2001). “Accelerators and Nobel Laureates”. Nobel Foundation. Truy cập ngày 31 tháng 1 năm 2008.
- ^ “The Nobel Prize in Physics 1990”. Nobel Foundation. ngày 17 tháng 10 năm 1990. Truy cập ngày 31 tháng 1 năm 2008.
- ^ Demtröder 2002, tr. 39–42.
- ^ Woan 2000, tr. 8.
- ^ MacGregor 1992, tr. 33–37.
- ^ a b Particle Data Group (2002). “The Particle Adventure”. Lawrence Berkeley Laboratory. Bản gốc lưu trữ ngày 4 tháng 1 năm 2007. Truy cập ngày 3 tháng 1 năm 2007.
- ^ a b Schombert, James (ngày 18 tháng 4 năm 2006). “Elementary Particles”. University of Oregon. Bản gốc lưu trữ ngày 30 tháng 8 năm 2011. Truy cập ngày 3 tháng 1 năm 2007.
- ^ Jevremovic 2005, tr. 63.
- ^ Pfeffer 2000, tr. 330–336.
- ^ Wenner, Jennifer M. (ngày 10 tháng 10 năm 2007). “How Does Radioactive Decay Work?”. Carleton College. Truy cập ngày 9 tháng 1 năm 2008.
- ^ a b c Raymond, David (ngày 7 tháng 4 năm 2006). “Nuclear Binding Energies”. New Mexico Tech. Bản gốc lưu trữ ngày 11 tháng 12 năm 2006. Truy cập ngày 3 tháng 1 năm 2007.
- ^ Mihos, Chris (ngày 23 tháng 7 năm 2002). “Overcoming the Coulomb Barrier”. Case Western Reserve University. Truy cập ngày 13 tháng 2 năm 2008.
- ^ Staff (ngày 30 tháng 3 năm 2007). “ABC's of Nuclear Science”. Lawrence Berkeley National Laboratory. Bản gốc lưu trữ ngày 5 tháng 12 năm 2006. Truy cập ngày 3 tháng 1 năm 2007.
- ^ Arjun Makhijani & Saleska, Scott (ngày 2 tháng 3 năm 2001). “Basics of Nuclear Physics and Fission”. Institute for Energy and Environmental Research. Bản gốc lưu trữ ngày 16 tháng 1 năm 2007. Truy cập ngày 3 tháng 1 năm 2007.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ Shultis & Faw 2002, tr. 10–17.
- ^ Fewell, M. P. (1995). “The atomic nuclide with the highest mean binding energy”. American Journal of Physics. 63 (7): 653–658. Bibcode:1995AmJPh..63..653F. doi:10.1119/1.17828.
- ^ Mulliken, Robert S. (1967). “Spectroscopy, Molecular Orbitals, and Chemical Bonding”. Science (journal). 157 (3784): 13–24. Bibcode:1967Sci...157...13M. doi:10.1126/science.157.3784.13. PMID 5338306.
- ^ a b Brucat, Philip J. (2008). “The Quantum Atom”. University of Florida. Bản gốc lưu trữ ngày 7 tháng 12 năm 2006. Truy cập ngày 4 tháng 1 năm 2007.
- ^ Manthey, David (2001). “Atomic Orbitals”. Orbital Central. Bản gốc lưu trữ ngày 10 tháng 1 năm 2008. Truy cập ngày 21 tháng 1 năm 2008.
- ^ Herter, Terry (2006). “Lecture 8: The Hydrogen Atom”. Cornell University. Truy cập ngày 14 tháng 2 năm 2008.
- ^ Bell, R. E.; Elliott, L. G. (1950). “Gamma-Rays from the Reaction H1(n,γ)D2 and the Binding Energy of the Deuteron”. Physical Review. 79 (2): 282–285. Bibcode:1950PhRv...79..282B. doi:10.1103/PhysRev.79.282.
- ^ Smirnov 2003, tr. 249–272.
- ^ Matis, Howard S. (ngày 9 tháng 8 năm 2000). “The Isotopes of Hydrogen”. Guide to the Nuclear Wall Chart. Lawrence Berkeley National Lab. Bản gốc lưu trữ ngày 18 tháng 12 năm 2007. Truy cập ngày 21 tháng 12 năm 2007.
- ^ Weiss, Rick (ngày 17 tháng 10 năm 2006). “Scientists Announce Creation of Atomic Element, the Heaviest Yet”. Washington Post. Truy cập ngày 21 tháng 12 năm 2007.
- ^ a b Sills 2003, tr. 131–134.
- ^ Dumé, Belle (ngày 23 tháng 4 năm 2003). “Bismuth breaks half-life record for alpha decay”. Physics World. Bản gốc lưu trữ ngày 14 tháng 12 năm 2007. Truy cập ngày 21 tháng 12 năm 2007.
- ^ Lindsay, Don (ngày 30 tháng 7 năm 2000). “Radioactives Missing From The Earth”. Don Lindsay Archive. Lưu trữ bản gốc ngày 28 tháng 4 năm 2007. Truy cập ngày 23 tháng 5 năm 2007.
- ^ Tuli, Jagdish K. (2005). “Nuclear Wallet Cards”. National Nuclear Data Center, Brookhaven National Laboratory. Truy cập ngày 16 tháng 4 năm 2011.
- ^ a b CRC Handbook (2002).
- ^ a b Mills (1993).
- ^ Chieh, Chung (ngày 22 tháng 1 năm 2001). “Nuclide Stability”. University of Waterloo. Bản gốc lưu trữ ngày 30 tháng 8 năm 2007. Truy cập ngày 4 tháng 1 năm 2007.
- ^ “Atomic Weights and Isotopic Compositions for All Elements”. National Institute of Standards and Technology. Bản gốc lưu trữ ngày 31 tháng 12 năm 2006. Truy cập ngày 4 tháng 1 năm 2007.
- ^ Audi, G.; Wapstra, A.H.; Thibault, C. (2003). “The Ame2003 atomic mass evaluation (II)”. Nuclear Physics A. 729 (1): 337–676. Bibcode:2003NuPhA.729..337A. doi:10.1016/j.nuclphysa.2003.11.003. Bản gốc lưu trữ ngày 16 tháng 9 năm 2008. Truy cập ngày 7 tháng 2 năm 2008.
- ^ Shannon, R. D. (1976). “Revised effective ionic radii and systematic studies of interatomic distances in halides and chalcogenides”. Acta Crystallographica A. 32 (5): 751. Bibcode:1976AcCrA..32..751S. doi:10.1107/S0567739476001551.
- ^ Dong, Judy (1998). “Diameter of an Atom”. The Physics Factbook. Bản gốc lưu trữ ngày 4 tháng 11 năm 2007. Truy cập ngày 19 tháng 11 năm 2007.
- ^ Zumdahl (2002).
- ^ Bethe, H. (1929). “Termaufspaltung in Kristallen”. Annalen der Physik, 5. Folge. 3: 133.
- ^ M. Birkholz & Rudert, R. (2008). “Interatomic distances in pyrite-structure disulfides – a case for ellipsoidal modeling of sulfur ions” (PDF). Physica status solidi b. 245 (9): 1858. Bibcode:2008PSSBR.245.1858B. doi:10.1002/pssb.200879532.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ Staff (2007). “Small Miracles: Harnessing nanotechnology”. Oregon State University. Truy cập ngày 7 tháng 1 năm 2007.—describes the width of a human hair as 105 nm and 10 carbon atoms as spanning 1 nm.
- ^ Padilla (2002:32)—"Có 2.000.000.000.000.000.000.000 nguyên tử oxy trong một giọt nước— và gấp hai lần số nguyên tử hydro."
- ^ Feynman 1995, tr. 5.
- ^ a b “Radioactivity”. Splung.com. Bản gốc lưu trữ ngày 4 tháng 12 năm 2007. Truy cập ngày 19 tháng 12 năm 2007.
- ^ L'Annunziata 2003, tr. 3–56.
- ^ Firestone, Richard B. (ngày 22 tháng 5 năm 2000). “Radioactive Decay Modes”. Berkeley Laboratory. Bản gốc lưu trữ ngày 29 tháng 9 năm 2006. Truy cập ngày 7 tháng 1 năm 2007.
- ^ Hornak, J. P. (2006). “Chapter 3: Spin Physics”. The Basics of NMR. Rochester Institute of Technology. Bản gốc lưu trữ ngày 3 tháng 2 năm 2007. Truy cập ngày 7 tháng 1 năm 2007.
- ^ a b Schroeder, Paul A. (ngày 25 tháng 2 năm 2000). “Magnetic Properties”. University of Georgia. Bản gốc lưu trữ ngày 29 tháng 4 năm 2007. Truy cập ngày 7 tháng 1 năm 2007.
- ^ Goebel, Greg (ngày 1 tháng 9 năm 2007). “[4.3] Magnetic Properties of the Atom”. Elementary Quantum Physics. In The Public Domain website. Truy cập ngày 7 tháng 1 năm 2007.
- ^ Yarris, Lynn (Spring 1997). “Talking Pictures”. Berkeley Lab Research Review. Bản gốc lưu trữ ngày 13 tháng 1 năm 2008. Truy cập ngày 9 tháng 1 năm 2008.
- ^ Liang & Haacke 1999, tr. 412–426.
- ^ Feynman, Richard; Leighton, Robert; Sands, Matthew (1965). “xem phần 2-5 về mức năng lượng, chương 19 về nguyên tử hydro”. The Feynman Lectures on Physics. 3. Addison Wesley (published 2005).
- ^ Zeghbroeck, Bart J. Van (1998). “Energy levels”. Shippensburg University. Bản gốc lưu trữ ngày 15 tháng 1 năm 2005. Truy cập ngày 23 tháng 12 năm 2007.
- ^ Feynman, Richard (2006). “3-Electrons and Their interactions”. QED: The strange theory of light and matter. Princeton University Press. ISBN 0-691-12575-9.
- ^ Fowles (1989:227–233).
- ^ W. C. Martin & Wiese, W. L. (2007). “Atomic Spectroscopy: A Compendium of Basic Ideas, Notation, Data, and Formulas”. National Institute of Standards and Technology. Bản gốc lưu trữ ngày 8 tháng 2 năm 2007. Truy cập ngày 8 tháng 1 năm 2007.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ “Atomic Emission Spectra — Origin of Spectral Lines”. Avogadro Web Site. Bản gốc lưu trữ ngày 28 tháng 2 năm 2006. Truy cập ngày 10 tháng 8 năm 2006.
- ^ Fitzpatrick, Richard (ngày 16 tháng 2 năm 2007). “Fine structure”. University of Texas at Austin. Truy cập ngày 14 tháng 2 năm 2008.
- ^ Weiss, Michael (2001). “The Zeeman Effect”. University of California-Riverside. Bản gốc lưu trữ ngày 2 tháng 2 năm 2008. Truy cập ngày 6 tháng 2 năm 2008.
- ^ Beyer 2003, tr. 232–236.
- ^ Watkins, Thayer. “Coherence in Stimulated Emission”. San José State University. Bản gốc lưu trữ ngày 12 tháng 1 năm 2008. Truy cập ngày 23 tháng 12 năm 2007.
- ^ Reusch, William (ngày 16 tháng 7 năm 2007). “Virtual Textbook of Organic Chemistry”. Michigan State University. Truy cập ngày 11 tháng 1 năm 2008.
- ^ “Covalent bonding – Single bonds”. chemguide. 2000.
- ^ Robert Husted (ngày 11 tháng 12 năm 2003). “Periodic Table of the Elements”. Los Alamos National Laboratory. Bản gốc lưu trữ ngày 10 tháng 1 năm 2008. Truy cập ngày 11 tháng 1 năm 2008.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ Baum, Rudy (2003). “It's Elemental: The Periodic Table”. Chemical & Engineering News. Truy cập ngày 11 tháng 1 năm 2008.
- ^ Goodstein 2002, tr. 436–438.
- ^ Brazhkin, Vadim V. (2006). “Metastable phases, phase transformations, and phase diagrams in physics and chemistry”. Physics-Uspekhi. 49 (7): 719–24. Bibcode:2006PhyU...49..719B. doi:10.1070/PU2006v049n07ABEH006013.
- ^ Marilyn Jacox & Gadzuk, J. William (1997). “Scanning Tunneling Microscope”. National Institute of Standards and Technology. Bản gốc lưu trữ ngày 7 tháng 1 năm 2008. Truy cập ngày 11 tháng 1 năm 2008.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ “The Nobel Prize in Physics 1986”. The Nobel Foundation. Truy cập ngày 11 tháng 1 năm 2008.—in particular, see the Nobel lecture by G. Binnig and H. Rohrer.
- ^ Jakubowski, N.; Moens, Luc; Vanhaecke, Frank (1998). “Sector field mass spectrometers in ICP-MS”. Spectrochimica Acta Part B: Atomic Spectroscopy. 53 (13): 1739–63. Bibcode:1998AcSpe..53.1739J. doi:10.1016/S0584-8547(98)00222-5.
- ^ Müller, Erwin W.; Panitz, John A.; McLane, S. Brooks (1968). “The Atom-Probe Field Ion Microscope”. Review of Scientific Instruments. 39 (1): 83–86. Bibcode:1968RScI...39...83M. doi:10.1063/1.1683116.
- ^ Jim Lochner;Gibb, Meredith; Newman, Phil (ngày 30 tháng 4 năm 2007). “What Do Spectra Tell Us?”. NASA/Goddard Space Flight Center. Bản gốc lưu trữ ngày 16 tháng 1 năm 2008. Truy cập ngày 3 tháng 1 năm 2008.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ Winter, Mark (2007). “Helium”. WebElements. Bản gốc lưu trữ ngày 30 tháng 12 năm 2007. Truy cập ngày 3 tháng 1 năm 2008.
- ^ “Planck reveals an almost perfect Universe”. ESA. ngày 21 tháng 3 năm 2013. Truy cập ngày 24 tháng 1 năm 2016.
- ^ Hinshaw, Gary (ngày 10 tháng 2 năm 2006). “What is the Universe Made Of?”. NASA/WMAP. Bản gốc lưu trữ ngày 31 tháng 12 năm 2007. Truy cập ngày 7 tháng 1 năm 2008.
- ^ Choppin, Liljenzin & Rydberg 2001, tr. 441.
- ^ Davidsen, Arthur F. (1993). “Far-Ultraviolet Astronomy on the Astro-1 Space Shuttle Mission”. Science. 259 (5093): 327–34. Bibcode:1993Sci...259..327D. doi:10.1126/science.259.5093.327. PMID 17832344.
- ^ Lequeux 2005, tr. 4.
- ^ Smith, Nigel (ngày 6 tháng 1 năm 2000). “The search for dark matter”. Physics World. Bản gốc lưu trữ ngày 16 tháng 2 năm 2008. Truy cập ngày 14 tháng 2 năm 2008.
- ^ Croswell, Ken (1991). “Boron, bumps and the Big Bang: Was matter spread evenly when the Universe began? Perhaps not; the clues lie in the creation of the lighter elements such as boron and beryllium”. New Scientist (1794): 42. Bản gốc lưu trữ ngày 7 tháng 2 năm 2008. Truy cập ngày 14 tháng 1 năm 2008.
- ^ Copi, Craig J.; Schramm, DN; Turner, MS (1995). “Big-Bang Nucleosynthesis and the Baryon Density of the Universe”. Science. 267 (5195): 192–99. arXiv:astro-ph/9407006. Bibcode:1995Sci...267..192C. doi:10.1126/science.7809624. PMID 7809624.
- ^ Hinshaw, Gary (ngày 15 tháng 12 năm 2005). “Tests of the Big Bang: The Light Elements”. NASA/WMAP. Bản gốc lưu trữ ngày 17 tháng 1 năm 2008. Truy cập ngày 13 tháng 1 năm 2008.
- ^ Abbott, Brian (ngày 30 tháng 5 năm 2007). “Microwave (WMAP) All-Sky Survey”. Hayden Planetarium. Truy cập ngày 13 tháng 1 năm 2008.
- ^ Hoyle, F. (1946). “The synthesis of the elements from hydrogen”. Monthly Notices of the Royal Astronomical Society. 106: 343–83. Bibcode:1946MNRAS.106..343H.
- ^ Knauth, D. C.; Knauth, D. C.; Lambert, David L.; Crane, P. (2000). “Newly synthesized lithium in the interstellar medium”. Nature. 405 (6787): 656–58. doi:10.1038/35015028. PMID 10864316.
- ^ Mashnik, Stepan G. (2000). "On Solar System and Cosmic Rays Nucleosynthesis and Spallation Processes". arΧiv:astro-ph/0008382 [astro-ph].
- ^ Manuel 2001, tr. 407–430, 511–519.
- ^ Dalrymple, G. Brent (2001). “The age of the Earth in the twentieth century: a problem (mostly) solved”. Geological Society, London, Special Publications. 190 (1): 205–21. Bibcode:2001GSLSP.190..205D. doi:10.1144/GSL.SP.2001.190.01.14. Truy cập ngày 14 tháng 1 năm 2008.
- ^ Don L. Anderson;Foulger, G. R.; Meibom, Anders (ngày 2 tháng 9 năm 2006). “Helium: Fundamental models”. MantlePlumes.org. Bản gốc lưu trữ ngày 8 tháng 2 năm 2007. Truy cập ngày 14 tháng 1 năm 2007.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ Pennicott, Katie (ngày 10 tháng 5 năm 2001). “Carbon clock could show the wrong time”. PhysicsWeb. Bản gốc lưu trữ ngày 15 tháng 12 năm 2007. Truy cập ngày 14 tháng 1 năm 2008.
- ^ Yarris, Lynn (ngày 27 tháng 7 năm 2001). “New Superheavy Elements 118 and 116 Discovered at Berkeley Lab”. Berkeley Lab. Bản gốc lưu trữ ngày 9 tháng 1 năm 2008. Truy cập ngày 14 tháng 1 năm 2008.
- ^ Diamond, H (1960). et al. “Heavy Isotope Abundances in Mike Thermonuclear Device”. Physical Review. 119 (6): 2000–04. Bibcode:1960PhRv..119.2000D. doi:10.1103/PhysRev.119.2000.
- ^ Poston Sr., John W. (ngày 23 tháng 3 năm 1998). “Do transuranic elements such as plutonium ever occur naturally?”. Scientific American. Truy cập ngày 15 tháng 1 năm 2008.
- ^ Keller, C. (1973). “Natural occurrence of lanthanides, actinides, and superheavy elements”. Chemiker Zeitung. 97 (10): 522–30. OSTI 4353086.
- ^ Zaider & Rossi 2001, tr. 17.
- ^ Manuel 2001, tr. 407–430,511–519.
- ^ “Oklo Fossil Reactors”. Curtin University of Technology. Bản gốc lưu trữ ngày 18 tháng 12 năm 2007. Truy cập ngày 15 tháng 1 năm 2008.
- ^ Weisenberger, Drew. “How many atoms are there in the world?”. Jefferson Lab. Truy cập ngày 16 tháng 1 năm 2008.
- ^ Pidwirny, Michael. “Fundamentals of Physical Geography”. University of British Columbia Okanagan. Bản gốc lưu trữ ngày 21 tháng 1 năm 2008. Truy cập ngày 16 tháng 1 năm 2008.
- ^ Anderson, Don L. (2002). “The inner inner core of Earth”. Proceedings of the National Academy of Sciences. 99 (22): 13966–68. Bibcode:2002PNAS...9913966A. doi:10.1073/pnas.232565899. PMC 137819. PMID 12391308.
- ^ Pauling, Linus (1960). The Nature of the Chemical Bond. Cornell University Press. tr. 5–10. ISBN 978-0-8014-0333-0. OCLC 17518275.
- ^ Anonymous (ngày 2 tháng 10 năm 2001). “Second postcard from the island of stability”. CERN Courier. Bản gốc lưu trữ ngày 3 tháng 2 năm 2008. Truy cập ngày 14 tháng 1 năm 2008.
- ^ Jacoby, Mitch (2006). “As-yet-unsynthesized superheavy atom should form a stable diatomic molecule with fluorine”. Chemical & Engineering News. 84 (10): 19. doi:10.1021/cen-v084n010.p019a.
- ^ Koppes, Steve (ngày 1 tháng 3 năm 1999). “Fermilab Physicists Find New Matter-Antimatter Asymmetry”. University of Chicago. Truy cập ngày 14 tháng 1 năm 2008.
- ^ Cromie, William J. (ngày 16 tháng 8 năm 2001). “A lifetime of trillionths of a second: Scientists explore antimatter”. Harvard University Gazette. Truy cập ngày 14 tháng 1 năm 2008.
- ^ Hijmans, Tom W. (2002). “Particle physics: Cold antihydrogen”. Nature. 419 (6906): 439–40. doi:10.1038/419439a. PMID 12368837.
- ^ Staff (ngày 30 tháng 10 năm 2002). “Researchers 'look inside' antimatter”. BBC News. Truy cập ngày 14 tháng 1 năm 2008.
- ^ Barrett, Roger (1990). “The Strange World of the Exotic Atom”. New Scientist (1728): 77–115. Bản gốc lưu trữ ngày 21 tháng 12 năm 2007. Truy cập ngày 4 tháng 1 năm 2008.
- ^ Indelicato, Paul (2004). “Exotic Atoms”. Physica Scripta. T112 (1): 20–26. arXiv:physics/0409058. Bibcode:2004PhST..112...20I. doi:10.1238/Physica.Topical.112a00020.
- ^ Ripin, Barrett H. (1998). “Recent Experiments on Exotic Atoms”. American Physical Society. Truy cập ngày 15 tháng 2 năm 2008.
Lỗi chú thích: Thẻ <ref> có tên “nist_bec” được định nghĩa trong <references> không được đoạn văn bản trên sử dụng.
Lỗi chú thích: Thẻ <ref> có tên “colton_fyffe1999” được định nghĩa trong <references> không được đoạn văn bản trên sử dụng.
<ref> có tên “kgs20050504” được định nghĩa trong <references> không được đoạn văn bản trên sử dụng.Sách tham khảo
[sửa | sửa mã nguồn]- L'Annunziata, Michael F. (2003). Handbook of Radioactivity Analysis. Academic Press. ISBN 0-12-436603-1. OCLC 16212955.
- Beyer, H. F. (2003). Introduction to the Physics of Highly Charged Ions. Shevelko, V. P. CRC Press. ISBN 0-7503-0481-2. OCLC 47150433.
- Choppin, Gregory R.; Liljenzin, Jan-Olov; Rydberg, Jan (2001). Radiochemistry and Nuclear Chemistry. Elsevier. ISBN 0-7506-7463-6. OCLC 162592180.
- Dalton, J. (1808). A New System of Chemical Philosophy, Part 1. London and Manchester: S. Russell.
- Demtröder, Wolfgang (2002). Atoms, Molecules and Photons: An Introduction to Atomic- Molecular- and Quantum Physics (ấn bản thứ 1). Springer. ISBN 3-540-20631-0. OCLC 181435713.
- Feynman, Richard (1995). Six Easy Pieces. The Penguin Group. ISBN 978-0-14-027666-4. OCLC 40499574.
- Fowles, Grant R. (1989). Introduction to Modern Optics. Courier Dover Publications. ISBN 0-486-65957-7. OCLC 18834711.
- Gangopadhyaya, Mrinalkanti (1981). Indian Atomism: History and Sources. Atlantic Highlands, New Jersey: Humanities Press. ISBN 0-391-02177-X. OCLC 10916778.
- Goodstein, David L. (2002). States of Matter. Courier Dover Publications. ISBN 0-13-843557-X.
- Harrison, Edward Robert (2003). Masks of the Universe: Changing Ideas on the Nature of the Cosmos. Cambridge University Press. ISBN 0-521-77351-2. OCLC 50441595.
- Iannone, A. Pablo (2001). Dictionary of World Philosophy. Routledge. ISBN 0-415-17995-5. OCLC 44541769.
- Jevremovic, Tatjana (2005). Nuclear Principles in Engineering. Springer. ISBN 0-387-23284-2. OCLC 228384008.
- King, Richard (1999). Indian philosophy: an introduction to Hindu and Buddhist thought. Edinburgh University Press. ISBN 0-7486-0954-7.
- Lequeux, James (2005). The Interstellar Medium. Springer. ISBN 3-540-21326-0. OCLC 133157789.
- Levere, Trevor, H. (2001). Transforming Matter – A History of Chemistry for Alchemy to the Buckyball. The Johns Hopkins University Press. ISBN 0-8018-6610-3.
- Liang, Z.-P.; Haacke, E. M. (1999). Webster, J. G. (biên tập). Encyclopedia of Electrical and Electronics Engineering: Magnetic Resonance Imaging (PDF). 2. John Wiley & Sons. tr. 412–26. ISBN 0-471-13946-7. Truy cập ngày 9 tháng 1 năm 2008.
- McEvilley, Thomas (2002). The shape of ancient thought: comparative studies in Greek and Indian philosophies. Allworth Press. ISBN 1-58115-203-5.
- MacGregor, Malcolm H. (1992). The Enigmatic Electron. Oxford University Press. ISBN 0-19-521833-7. OCLC 223372888.
- Manuel, Oliver (2001). Origin of Elements in the Solar System: Implications of Post-1957 Observations. Springer. ISBN 0-306-46562-0. OCLC 228374906.
- Mazo, Robert M. (2002). Brownian Motion: Fluctuations, Dynamics, and Applications. Oxford University Press. ISBN 0-19-851567-7. OCLC 48753074.
- Mills, Ian (1993). Quantities, Units and Symbols in Physical Chemistry. Cvitaš, Tomislav; Homann, Klaus; Kallay, Nikola; Kuchitsu, Kozo (ấn bản thứ 2). Oxford: International Union of Pure and Applied Chemistry, Commission on Physiochemical Symbols Terminology and Units, Blackwell Scientific Publications. ISBN 0-632-03583-8. OCLC 27011505.
- Moran, Bruce T. (2005). Distilling Knowledge: Alchemy, Chemistry, and the Scientific Revolution. Harvard University Press. ISBN 0-674-01495-2.
- Myers, Richard (2003). The Basics of Chemistry. Greenwood Press. ISBN 0-313-31664-3. OCLC 50164580.
- Padilla, Michael J. (2002). Prentice Hall Science Explorer: Chemical Building Blocks. Miaoulis, Ioannis; Cyr, Martha. Upper Saddle River, New Jersey USA: Prentice-Hall, Inc. ISBN 0-13-054091-9. OCLC 47925884.
- Pais, Abraham (1986). Inward Bound: Of Matter and Forces in the Physical World. New York: Oxford University Press. ISBN 0-19-851971-0.
- Pauling, Linus (1960). The Nature of the Chemical Bond. Cornell University Press. ISBN 0-8014-0333-2. OCLC 17518275.
- Pfeffer, Jeremy I. (2000). Modern Physics: An Introductory Text. Nir, Shlomo. Imperial College Press. ISBN 1-86094-250-4. OCLC 45900880.
- Ponomarev, Leonid Ivanovich (1993). The Quantum Dice. CRC Press. ISBN 0-7503-0251-8. OCLC 26853108.
- Roscoe, Henry Enfield (1895). John Dalton and the Rise of Modern Chemistry. Century science series. New York: Macmillan. Truy cập ngày 3 tháng 4 năm 2011.
- Scerri, Eric R. (2007). The periodic table: its story and its significance. Oxford University Press US. ISBN 0-19-530573-6.
- Shultis, J. Kenneth; Faw, Richard E. (2002). Fundamentals of Nuclear Science and Engineering. CRC Press. ISBN 0-8247-0834-2. OCLC 123346507.
- Siegfried, Robert (2002). From Elements to Atoms: A History of Chemical Composition. DIANE. ISBN 0-87169-924-9. OCLC 186607849.
- Sills, Alan D. (2003). Earth Science the Easy Way. Barron's Educational Series. ISBN 0-7641-2146-4. OCLC 51543743.
- Smirnov, Boris M. (2003). Physics of Atoms and Ions. Springer. ISBN 0-387-95550-X.
- Teresi, Dick (2003). Lost Discoveries: The Ancient Roots of Modern Science. Simon & Schuster. tr. 213–214. ISBN 0-7432-4379-X.
- Various (2002). Lide, David R. (biên tập). Handbook of Chemistry & Physics (ấn bản thứ 88). CRC. ISBN 0-8493-0486-5. OCLC 179976746. Bản gốc lưu trữ ngày 23 tháng 5 năm 2008. Truy cập ngày 23 tháng 5 năm 2008.
- Woan, Graham (2000). The Cambridge Handbook of Physics. Cambridge University Press. ISBN 0-521-57507-9. OCLC 224032426.
- Wurtz, Charles Adolphe (1881). The Atomic Theory. New York: D. Appleton and company. ISBN 0-559-43636-X.
- Zaider, Marco; Rossi, Harald H. (2001). Radiation Science for Physicians and Public Health Workers. Springer. ISBN 0-306-46403-9. OCLC 44110319.
- Zumdahl, Steven S. (2002). Introductory Chemistry: A Foundation (ấn bản thứ 5). Houghton Mifflin. ISBN 0-618-34342-3. OCLC 173081482. Bản gốc lưu trữ ngày 4 tháng 3 năm 2008. Truy cập ngày 5 tháng 2 năm 2008.
Liên kết ngoài
[sửa | sửa mã nguồn]| Wikimedia Commons có thêm hình ảnh và phương tiện truyền tải về Nguyên tử. |
- Atom tại Encyclopædia Britannica (tiếng Anh)
- Nguyên tử tại Từ điển bách khoa Việt Nam
- Cấu trúc của nguyên tử bản lưu Quantum Mechanics 22/4/2004
- Francis, Eden (2002). “Atomic Size”. Clackamas Community College. Bản gốc lưu trữ ngày 4 tháng 2 năm 2007. Truy cập ngày 9 tháng 1 năm 2007.
- Freudenrich, Craig C. “How Atoms Work”. How Stuff Works. Truy cập ngày 9 tháng 1 năm 2007.
- “Atom:The Atom”. Free High School Science Texts: Physics. Wikibooks. Bản gốc lưu trữ ngày 13 tháng 6 năm 2006. Truy cập ngày 9 tháng 1 năm 2007.
- Anonymous (2007). “The atom”. Science aid+. Bản gốc lưu trữ ngày 22 tháng 7 năm 2011. Truy cập ngày 9 tháng 1 năm 2007.—a guide to the atom for teens.
- Anonymous (ngày 3 tháng 1 năm 2006). “Atoms and Atomic Structure”. BBC. Truy cập ngày 11 tháng 1 năm 2007.
- Various (ngày 3 tháng 1 năm 2006). “Physics 2000, Table of Contents”. University of Colorado. Bản gốc lưu trữ ngày 14 tháng 1 năm 2008. Truy cập ngày 11 tháng 1 năm 2008.
- Various (ngày 3 tháng 2 năm 2006). “What does an atom look like?”. University of Karlsruhe. Bản gốc lưu trữ ngày 17 tháng 4 năm 2010. Truy cập ngày 12 tháng 5 năm 2008.

