Zirconi(IV) chloride
| Zirconi(IV) chloride | |
|---|---|
 | |
 | |
 | |
| Danh pháp IUPAC | Zirconium tetrachloride Zirconium(IV) chloride |
| Tên khác | Zirconi tetrachloride |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| Số EINECS | |
| ChEBI | |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| UNII | |
| Thuộc tính | |
| Công thức phân tử | ZrCl4 |
| Khối lượng mol | 233,0348 g/mol |
| Bề ngoài | Tinh thể trắng hút ẩm |
| Khối lượng riêng | 2,8 g/cm³ |
| Điểm nóng chảy | 437 °C (710 K; 819 °F) |
| Điểm sôi | 331 °C (604 K; 628 °F) (thăng hoa) |
| Độ hòa tan trong nước | thủy phân |
| Độ hòa tan | tan trong alcohol, ether, HCl tạo phức với amonia |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
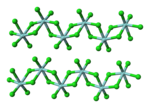
Zirconi(IV) chloride, còn được gọi với cái tên khác là zirconi tetrachloride, là một hợp chất vô cơ có thành phần gồm hai nguyên tố zirconi và clo, với công thức hóa học được quy định là ZrCl4. Hợp chất này thường được sử dụng làm tiền chất cho các hợp chất khác của nguyên tố zirconi. Hợp chất này là một chất rắn nóng chảy nhanh chóng, ngoài ra cũng thủy phân nhanh chóng trong không khí ẩm.
Các ứng dụng
[sửa | sửa mã nguồn]Tiền thân của Zr kim loại
[sửa | sửa mã nguồn]ZrCl4 là một chất trung gian trong việc chuyển đổi các khoáng chất zirconi thành zirconi kim loại theo quy trình Kroll. Trong tự nhiên, nguyên tố zirconium luôn tồn tại dưới dạng oxit. Đối với việc chuyển đổi sang kim loại nguyên chất các oxit chịu lửa này phải được được chuyển đổi thành hợp chất tetrachloride và có thể được chưng cất ở nhiệt độ cao. Các tinh thể ZrCl4 tinh khiết có thể được khử với kim loại Zr để sản xuất hợp chất zirconi(III) chloride.
Sử dụng khác
[sửa | sửa mã nguồn]ZrCl4 là tiền chất phổ biến nhất đối với sự lắng đọng hơi hóa học của zirconi(IV) oxit và zirconi điborua.[1]
Trong tổng hợp hữu cơ, zirconi tetrachloride được sử dụng như là một axit Lewis yếu cho phản ứng Friedel-Crafts, phản ứng Diels-Alder và các phản ứng đóng vòng hóa phân tử.[2] Nó cũng được sử dụng để điều trị chống thấm nước hàng dệt may và các vật liệu dạng xơ khác.
Hợp chất khác
[sửa | sửa mã nguồn]ZrCl4 còn tạo ra một số hợp chất với NH3, như:
- ZrCl4·2NH3;
- ZrCl4·4NH3;
- ZrCl4·8NH3.
Chúng đều là bột màu trắng.[3]
Tham khảo
[sửa | sửa mã nguồn]- ^ Randich, E. (ngày 1 tháng 11 năm 1979). “Chemical vapor deposited borides of the form (Ti,Zr)B2 and (Ta,Ti)B2”. Thin Solid Films. 63 (2): 309–313. Bibcode:1979TSF....63..309R. doi:10.1016/0040-6090(79)90034-8.
- ^ Bora U. (2003). “Zirconium Tetrachloride”. Synlett (7): 1073–1074. doi:10.1055/s-2003-39323.
- ^ Crookes, William; Gardiner, James H.; Druce, Gerald; Ryan, H. W. Blood (1899). The Chemical News and Journal of Industrial Science: With which is Incorporated the "Chemical Gazette". A Journal of Practical Chemistry in All Its Applications to Pharmacy, Arts and Manufactures (bằng tiếng Anh). Chemical news office. tr. 15–16.
