Natri oxybate
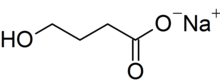 | |
| Dữ liệu lâm sàng | |
|---|---|
| Tên thương mại | Alcover, Gamma-OH, Natrii oxybutyras Kalceks, Somsanit, Xyrem[1] |
| Đồng nghĩa | NSC-84223, WY-3478 |
| AHFS/Drugs.com | Chuyên khảo |
| MedlinePlus | a605032 |
| Giấy phép | |
| Danh mục cho thai kỳ |
|
| Dược đồ sử dụng | Oral |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý |
|
| Dữ liệu dược động học | |
| Sinh khả dụng | 88%[2] |
| Liên kết protein huyết tương | <1%[2] |
| Chu kỳ bán rã sinh học | 0.5 to 1 hour. |
| Bài tiết | Almost entirely by biotransformation to carbon dioxide, which is then eliminated by expiration |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| PubChem SID | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| KEGG | |
| ChEMBL | |
| ECHA InfoCard | 100.007.231 |
| Dữ liệu hóa lý | |
| Công thức hóa học | C4H7NaO3 |
| Khối lượng phân tử | 126.09 g/mol |
| Mẫu 3D (Jmol) | |
SMILES
| |
Định danh hóa học quốc tế
| |
| (kiểm chứng) | |
Natri oxybate là một loại thuốc theo toa được sử dụng để điều trị hai triệu chứng chứng ngủ rũ: yếu cơ đột ngột và buồn ngủ ban ngày quá mức.[3] Nó được sử dụng đôi khi ở Pháp và Ý như một thuốc gây mê tiêm tĩnh mạch;[4] :15, 27–28 nó cũng được sử dụng ở Ý để điều trị chứng nghiện rượu và hội chứng cai rượu.[5]
Natri oxybate là muối natri của axit-hydroxybutyric (GHB). Các thử nghiệm lâm sàng đối với chứng ngủ rũ được thực hiện giống như lạm dụng GHB như một loại thuốc câu lạc bộ và thuốc hiếp dâm ngày trở thành vấn đề được công chúng quan tâm; vào năm 2000 GHB đã được tạo ra một chất được kiểm soát theo Lịch I, trong khi natri oxybate, khi được sử dụng theo FDA NDA hoặc IND, được phân loại là chất được kiểm soát theo Lịch III để sử dụng thuốc theo Đạo luật về các chất bị kiểm soát, với việc sử dụng bất hợp pháp theo hình phạt của Biểu I. [6]
Natri oxybate đã được FDA chấp thuận sử dụng để điều trị các triệu chứng chứng ngủ rũ vào năm 2002 với chương trình đánh giá rủi ro và giảm thiểu rủi ro nghiêm ngặt (REMS) do FDA ủy quyền. Nhãn hiệu natri oxybate của Mỹ cũng có cảnh báo hộp đen vì đây là thuốc ức chế hệ thần kinh trung ương và có thể gây ức chế hô hấp, co giật, hôn mê hoặc tử vong, đặc biệt nếu được sử dụng kết hợp với các thuốc ức chế thần kinh trung ương khác, như rượu và việc sử dụng nó có thể gây ra sự phụ thuộc.Ở Canada và Liên minh châu Âu (EU), nó được phân loại lần lượt là Chất kiểm soát III và Bảng IV.[7]
Nó đã được phê duyệt để điều trị các triệu chứng chứng ngủ rũ ở châu Âu vào năm 2005.[3]
Orphan Medical đã phát triển nó và được Jazz Pharmaceuticals mua lại vào năm 2005. Thuốc được bán ra ở châu Âu bởi UCB. Jazz đã tăng giá thuốc một cách đáng kể sau khi mua lại Orphan,[8] và trả khoản tiền phạt 20 triệu đô la cho việc tiếp thị ngoài nhãn thuốc vào năm 2007 [9]
Sử dụng y tế
[sửa | sửa mã nguồn]Sử dụng lâm sàng natri oxybate đã được giới thiệu ở châu Âu vào năm 1964 dưới dạng thuốc gây tê tiêm tĩnh mạch nhưng nó không được sử dụng rộng rãi vì đôi khi nó gây ra cơn động kinh; cho đến năm 2006 nó vẫn được phép sử dụng ở Pháp và Ý nhưng không được sử dụng rộng rãi.[4] :15,27–28
Công dụng chính của natri oxybate là điều trị hai trong số các triệu chứng của chứng ngủ rũ – cataplexy (yếu cơ đột ngột) và buồn ngủ ban ngày quá mức. Nhận xét của natri oxybate kết luận rằng nó được dung nạp tốt và gắn liền với "giảm đáng kể trong cataplexy và ban ngày buồn ngủ," [10] và hiệu quả của nó "trong điều trị lớn, các triệu chứng ngủ rũ có liên quan về mặt lâm sàng và bất thường về cấu trúc giấc ngủ" đã được thành lập.[11] Tuy nhiên, do các rủi ro lạm dụng liên quan đến thuốc này, nó chỉ có sẵn ở Hoa Kỳ thông qua chương trình đánh giá và giảm thiểu rủi ro (REMS) do FDA ủy quyền. Chương trình yêu cầu các nhà cung cấp kê đơn thuốc phải được chứng nhận để làm như vậy, rằng nó chỉ được phân phối từ một nhà thuốc trung tâm được chứng nhận để làm như vậy, và những người được kê đơn phải đăng ký vào một chương trình cho thuốc và phải ghi lại rằng họ đang sử dụng thuốc an toàn.
Trong thời gian gần đây, các cuộc điều tra về việc sử dụng nó trong việc đối phó với hội chứng cai rượu đã bắt đầu. Chúng bắt đầu ở Ý, nơi mà việc sử dụng nó trong điều trị nghiện rượu cũng được khám phá; bằng chứng cho những sử dụng này là yếu [4] :15,28–29 [5] nhưng đang phát triển và nó cũng đã được phê duyệt để sử dụng ở Áo.[12] Không đủ bằng chứng để so sánh dứt khoát với các phương pháp điều trị dựa trên clomethiazole hoặc benzodiazepine, mặc dù một số dữ liệu cho thấy nó có thể "tốt hơn naltrexone và disulfiram về duy trì kiêng khem và phòng ngừa thèm thuốc trong trung hạn 3-12 tháng." [13] Trong một đánh giá năm 2014, Gillian Keat đã mô tả natri oxybate là một "lựa chọn hữu ích để điều trị hội chứng cai rượu và duy trì cai nghiện rượu." Tuy nhiên, một đánh giá năm 2018 đã công nhận bằng chứng về hiệu quả của nó nhưng lưu ý những lo ngại về an toàn và kết luận rằng "các nghiên cứu vẫn còn hạn chế và cần phải điều tra bao gồm số lượng bệnh nhân lớn hơn".[14]
Phụ nữ mang thai không nên dùng nó, và phụ nữ không nên mang thai trong khi dùng. Nó được bài tiết qua sữa mẹ và không nên được sử dụng bởi các bà mẹ cho con bú.[3]
Tác dụng phụ
[sửa | sửa mã nguồn]Nhãn Mỹ cho natri oxybate có cảnh báo hộp đen vì đây là thuốc ức chế hệ thần kinh trung ương (thuốc ức chế thần kinh trung ương) và vì khả năng lạm dụng. Các tác dụng phụ tiềm ẩn khác bao gồm ức chế hô hấp, co giật, hôn mê và tử vong, đặc biệt là khi dùng chung với các thuốc ức chế thần kinh trung ương khác như rượu.[15] Các trường hợp phụ thuộc nghiêm trọng và thèm thuốc đã được báo cáo với việc sử dụng quá mức và bất hợp pháp của thuốc này.[16][17] GHB, dạng proton (axit) của muối này, đã được sử dụng để thực hiện tấn công tình dục và hiếp dâm được tạo điều kiện bằng thuốc,[18][19] mặc dù dạng GHB bất hợp pháp thường có các đặc điểm khác với dược phẩm natri oxybate hồi phục.[20]
Nó gây chóng mặt, buồn nôn và đau đầu ở 10% đến 20% những người dùng nó; buồn nôn phổ biến ở phụ nữ hơn nam giới.[3][21]
Từ 1% đến 10% số người bị nghẹt mũi, chảy nước mũi hoặc đau họng, chán ăn, cảm giác bị bóp méo, cataplexy, yếu đuối, lo lắng hoặc lo lắng, tâm trạng chán nản, ác mộng hoặc giấc mơ bất thường, tê liệt khi ngủ rối loạn giấc ngủ khác bao gồm mất ngủ, buồn ngủ hoặc an thần, té ngã, chóng mặt, run, rối loạn thăng bằng, các vấn đề nhận thức bao gồm rối loạn chú ý, nhầm lẫn hoặc mất phương hướng, cảm giác tê liệt, ngứa ran, mờ mắt, tim đập nhanh, huyết áp cao, khó thở, ngáy, nôn, tiêu chảy, đau dạ dày, đổ mồ hôi nhiều, phát ban, đau khớp, đau cơ, đau lưng, co thắt cơ, đái dầm, tiểu không tự chủ và sưng chân tay.[3]
Quá liều
[sửa | sửa mã nguồn]Các báo cáo về quá liều trong tài liệu y khoa nói chung là do lạm dụng, và thường liên quan đến các loại thuốc khác. Các triệu chứng bao gồm nôn mửa, đổ mồ hôi quá nhiều, hôn mê, thời gian ngừng thở, co giật, kích động, mất các kỹ năng tâm lý và hôn mê. Quá liều có thể dẫn đến tử vong do suy hô hấp. Những người dùng quá liều có thể chết vì ngạt do nôn mửa của chính họ. Những người đã sử dụng quá liều hoặc nghi ngờ quá liều có thể cần phải được thực hiện để nôn, đặt nội khí quản hoặc / và đặt mặt nạ phòng độc.[3]
Tương tác
[sửa | sửa mã nguồn]Nó không nên được sử dụng với các loại thuốc khác là thuốc ức chế thần kinh trung ương như rượu hoặc thuốc an thần. Sử dụng với divalproex cho kết quả tăng khoảng 25% khả dụng của natri oxybate.
Dược lý
[sửa | sửa mã nguồn]Cơ chế hoạt động của natri oxybate vẫn chưa được biết.[3] GHB là một chất chuyển hóa bình thường của GABA tương tác với thụ thể GABAB.
Nó được hấp thu nhanh chóng và có khoảng 88% sinh khả dụng; rất ít liên kết với protein huyết tương. Thời gian trung bình đến nồng độ đỉnh trong huyết tương dao động từ 0,5 đến 1,25 giờ. Rất ít thuốc được bài tiết; thay vào đó, nó chủ yếu được chuyển hóa qua một số bước thành carbon dioxide và nước.
Hóa học
[sửa | sửa mã nguồn]Sodium oxybate là natri muối của axit γ-hydroxybutyric (GHB). Tên hóa học có hệ thống của nó là natri 4 hydroxybutanoate, mặc dù từ đồng nghĩa như natri γ -hydroxybutyrate được sử dụng phổ biến. Công thức cấu trúc cô đặc của nó là HOCH
2CH
2CH
2CO
2Na (công thức phân tử: C
4H
7NaO
3) và khối lượng mol của nó là 126,09 g mol − 1. Nó rất ưa nước. Xử lý muối bằng axit cho phép thu hồi dạng axit cacboxylic của hợp chất, đó là GHB.
Lịch sử
[sửa | sửa mã nguồn]
Alexander Zaytsev làm việc về gia đình hóa học này và công bố công trình về nó vào năm 1874.[22] :79 [23] Nghiên cứu mở rộng đầu tiên về GHB và việc sử dụng nó ở người được tiến hành vào đầu những năm 1960 bởi Tiến sĩ Henri Labit để sử dụng trong nghiên cứu chất dẫn truyền thần kinh GABA.[4] :11–12 [24] Nó được nghiên cứu trong một loạt các ứng dụng bao gồm phẫu thuật sản khoa và trong khi sinh con và như là một giải lo âu; đã có những báo cáo giai thoại về việc nó có tác dụng chống trầm cảm và kích thích tình dục. :27 Nó cũng được nghiên cứu như một chất gây mê nội nhãn và được bán trên thị trường cho mục đích đó bắt đầu từ năm 1964 ở châu Âu nhưng nó không được sử dụng rộng rãi vì nó gây ra động kinh; kể từ năm 2006, việc sử dụng đó vẫn được cho phép ở Pháp và Ý nhưng không được sử dụng rộng rãi. :27–28 GHB cũng được nghiên cứu để điều trị chứng nghiện rượu :28–29 và được sử dụng trong chứng ngủ rũ từ những năm 1960 trở đi. :28
Vào tháng 5 năm 1990 GHB đã được giới thiệu như một chất bổ sung chế độ ăn uống và được bán cho các nhà xây dựng cơ thể, để giúp kiểm soát cân nặng và hỗ trợ giấc ngủ, và như một "thay thế" cho L -tryptophan, đã bị loại khỏi thị trường vào tháng 11 năm 1989 khi các đợt của nó đã được tìm thấy để gây ra hội chứng tăng bạch cầu ái toan. Đến tháng 11 năm đó, 57 trường hợp mắc bệnh do bổ sung GHB đã được báo cáo cho Trung tâm kiểm soát và phòng ngừa dịch bệnh, với những người đã uống tới ba muỗng cà phê GHB; không có trường hợp tử vong nhưng chín người cần được chăm sóc trong phòng chăm sóc đặc biệt.[25][26] FDA đã đưa ra cảnh báo vào tháng 11 năm 1990 rằng việc bán GHB là bất hợp pháp. GHB tiếp tục được sản xuất và bán bất hợp pháp và nó và các chất tương tự đã được sử dụng như một loại thuốc câu lạc bộ và được sử dụng như một loại thuốc hiếp dâm ngày. DEA đã có những cơn co giật và FDA đã đưa ra cảnh báo nhiều lần trong suốt những năm 1990.[27][28][29]
Đồng thời, nghiên cứu về việc sử dụng GHB dưới dạng natri oxybate đã được chính thức hóa, vì một công ty tên là Orphan Medical Inc. đã nộp đơn đăng ký nghiên cứu thuốc mới và đang tiến hành thử nghiệm lâm sàng với ý định đạt được sự chấp thuận theo quy định để sử dụng điều trị chứng ngủ rũ.[4] :18–25;28 [30] :10 Năm 1996, Orphan ký hợp đồng với Lonza Group, một nhà sản xuất hợp đồng cung cấp thuốc.[31]
Năm 2000, Đạo luật phòng chống hiếp dâm ngày 2000 của Hillory J. Farias và Samantha Reid đã được ký kết thành luật tại Hoa Kỳ, điều này đã tạo ra GHB theo Biểu I của Đạo luật về các chất bị kiểm soát, nhưng natri oxybate, khi được sử dụng theo IND hoặc NDA từ FDA Hoa Kỳ, được coi là chất Lịch III nhưng với hình phạt buôn bán theo Lịch trình I.[32][33]
Nó đã được FDA chấp thuận vào năm 2002 dưới tên thương mại Xyrem với chiến lược kiểm soát rủi ro nghiêm ngặt nhằm ngăn chặn sự phân tán thuốc và kiểm soát nguy cơ lạm dụng bởi những người được kê đơn.[34]
Orphan Medical đã cấp phép bán thuốc ở Châu Âu cho Celltech vào năm 2003.[35][36] Năm 2004, CellTech đã được mua lại bởi UCB [37] và năm 2005 Jazz Pharmaceuticals đã mua lại Orphan Medical.[38]
Vào tháng 1 năm 2007, Valeant đã thông báo rằng Jazz đã cấp phép cho thị trường Xyrem ở Canada cho Valeant.[39]
Vào tháng 7 năm 2007, Jazz và công ty con Orphan Medical của họ đã nhận tội hình sự về tội nghiêm trọng trong việc tiếp thị natri oxybate; họ cũng giải quyết một vụ kiện dân sự cùng một lúc. Vấn đề đã được đưa ra bởi một cựu đại diện bán hàng, người đã đệ trình một trường hợp qui tam chống lại công ty theo Đạo luật Yêu cầu Sai. Đại diện bán hàng đã gọi điện cho các bác sĩ không điều trị cho người mắc chứng ngủ rũ và nói với họ về những công dụng tiềm năng của thuốc bao gồm mệt mỏi, mất ngủ, đau mãn tính, giảm cân, trầm cảm, rối loạn lưỡng cực và rối loạn vận động như bệnh Parkinson và hạ thấp rủi ro được mô tả trong cảnh báo hộp đen của nhãn. Một người quản lý bán hàng đã tham gia vào kế hoạch tiếp thị bất hợp pháp trước đó đã nhận tội và một bác sĩ tâm thần đã quảng cáo thuốc này đã bị buộc tội trước đó. Jazz đã trả tổng cộng 20 triệu đô la và đồng ý với thỏa thuận liêm chính của công ty và thực hiện cải cách nội bộ.[9][40][41]
FDA đã gửi cho Jazz một bức thư cảnh báo của FDA về các vi phạm an toàn vào tháng 9 năm 2007 [42]
Vào năm 2010, FDA đã từ chối Ứng dụng Thuốc mới của Jazz vì sử dụng natri oxybate trong chứng đau cơ xơ hóa.[43]
Vào tháng 10 năm 2011, FDA đã gửi cho Jazz một bức thư cảnh báo khác của FDA về việc không thu thập, đánh giá và báo cáo kịp thời các tác dụng phụ cho FDA sau khi hãng bắt đầu tiếp thị thuốc.[42] Nó đã gửi một bức thư khác vào năm 2013 nói rằng các vấn đề được mô tả trong bức thư năm 2011 dường như đã được giải quyết.[44]
Vào tháng 1 năm 2017, FDA đã phê duyệt sản phẩm natri oxybate chung đầu tiên cho các triệu chứng chứng ngủ rũ, cũng phải tuân theo các điều kiện chương trình REMS giống như ban đầu.[45] Đến tháng 4 năm 2017, 7 công ty đã đệ trình ANDAs với FDA để đưa ra thị trường các phiên bản chung của Xyrem và Jazz đã đệ trình các trường hợp vi phạm bằng sáng chế chống lại họ. Hikma Pharmaceuticals đã là công ty đầu tiên nộp ANDA và Jazz đã giải quyết với họ vào tháng 4 năm 2017; theo thỏa thuận, Hikma có thể bắt đầu bán một loại thuốc được ủy quyền vào năm 2023 theo Jazz 'REMS và sẽ có năm năm độc quyền, tuy nhiên những điều kiện đó có thể thay đổi nếu bằng sáng chế của Jazz bị vô hiệu.[46][47]
Vào năm 2017, Jazz và Valeant đã chấm dứt thỏa thuận, theo đó Valete tiếp thị Xyrem ở Canada.[48]
Xã hội và văn hoá
[sửa | sửa mã nguồn]Quy định
[sửa | sửa mã nguồn]Ở Mỹ, GHB là chất được kiểm soát theo Lịch I, trong khi natri oxybate, khi được sử dụng theo FDA NDA hoặc IND, được phân loại là chất được kiểm soát theo Lịch III để sử dụng thuốc theo Đạo luật về các chất bị kiểm soát, với việc sử dụng bất hợp pháp theo Hình phạt I.[6]
Tại Canada và Liên minh châu Âu (EU), tính đến năm 2009, nó đã được phân loại lần lượt là Chất kiểm soát III và Bảng IV.[7]
Giá cả
[sửa | sửa mã nguồn]Tại Hoa Kỳ, chi phí (tính đến quý 3 năm 2015) của Xyrem là 5,468,09 đô la cho mỗi chai 180 mL (500 mg / mL) (cung cấp 10 đến 15 ngày). Tính đến năm 2017, chi phí natri oxybate ở Anh là £ 540,00 đến £ 1,080 cho nguồn cung cấp ba mươi ngày,[49] với liều thông thường là £ 6.500 đến £ 13.100 mỗi năm.[50]
Jazz Pharmaceuticals đã tăng giá Xyrem 841%, kiếm được tổng cộng 569 triệu đô la trong năm 2013 và chiếm hơn 50% doanh thu của Jazz Pharmaceuticals.[8] Năm 2007 có giá 2,04 đô la; vào năm 2014, chi phí $ 19,40 mỗi liều 1 ml. Jazz cung cấp hỗ trợ đồng thanh toán để giúp bệnh nhân tiếp cận với loại thuốc đắt tiền. Theo DRX, một báo cáo dữ liệu thuốc do Bloomberg công bố, Jazz Pharmaceuticals tăng giá trên Xyrem đứng đầu danh sách tăng giá trong năm 2014.
Trong lịch sử, thuốc mồ côi có giá cao hơn các loại thuốc khác và đã được điều trị đặc biệt kể từ khi ban hành Đạo luật về thuốc mồ côi của Mỹ năm 1983. Tuy nhiên, những đợt tăng giá mạnh của trẻ mồ côi và các loại thuốc đặc trị khác đã được xem xét kỹ lưỡng.[8] Chi phí trung bình của một loại thuốc đặc trị ở Mỹ là 65.000 đô la hàng năm vào tháng 6 năm 2013 (khoảng 5.416 đô la một tháng). Giá của Xyrem ở Mỹ đã tăng trung bình 40% mỗi năm kể từ khi nó trở nên có sẵn như một đơn thuốc.[51]
Tại các quốc gia thuộc Liên minh Châu Âu (EU), chính phủ cung cấp bảo hiểm y tế quốc gia (như ở Anh và Ý) hoặc quy định chặt chẽ các quỹ bảo hiểm xã hội bán tư nhân (như ở Đức, Pháp và Hà Lan). Các cơ quan chính phủ này là người mua duy nhất (hoặc cơ quan quản lý) hàng hóa và dịch vụ y tế và có quyền định giá.[52] Chi phí dược phẩm, bao gồm natri oxybate, có xu hướng thấp hơn ở các quốc gia này.
NHS Anh ủy quyền và thanh toán cho natri oxybate bằng các yêu cầu tài trợ cá nhân trên cơ sở các trường hợp đặc biệt. Bộ Y tế Anh trả tiền thuốc cho 80 bệnh nhân đang có hành động pháp lý đối với các vấn đề liên quan đến việc sử dụng vắc-xin cúm lợn Pandemrix với chi phí 12.000 bảng mỗi năm. Tính đến năm 2016, có nhiều khu vực ở Anh, nơi NHS không trả tiền cho nó.[53][54] Vào tháng 5 năm 2016, họ đã được Tòa án tối cao ra lệnh cung cấp kinh phí để điều trị cho một thiếu niên mắc chứng ngủ rũ nặng. Thẩm phán đã chỉ trích chính sách quyết định tồi tệ của họ và chính sách phi lý của họ đối với cô gái khi hàng trăm bệnh nhân NHS khác đã nhận được thuốc.[55]
Tên gọi
[sửa | sửa mã nguồn]Natri oxybate là tên gọi chung của hóa chất; nó không có INN.[56]
Kể từ tháng 4 năm 2018, natri oxybarate đã được bán dưới các nhãn hiệu sau: Alcover (Ý), Gamma-OH (Pháp), Natrii oxybutyras Kalceks (Latvia), Somsanit (Đức), Xyrem (nhiều quốc gia của Jazz và UCB).[1]
Nghiên cứu
[sửa | sửa mã nguồn]Natri oxybate cần được cung cấp trong đêm; như năm 2017 nghiên cứu đã được thực hiện để tạo ra các công thức sẽ kéo dài suốt đêm.[57]
Jazz đã phát triển JZP-386, một deuterated analog natri oxybate. Công ty đã trình bày kết quả giai đoạn I vào năm 2015, nói rằng các tác dụng liên quan đến deuterium khiến nó cần thiết phải thực hiện công việc tiếp theo như là một phần của sự phát triển của thuốc.[58]
Tham khảo
[sửa | sửa mã nguồn]- ^ a b “International brands for Sodium Oxybate -”. Drugs.com. Truy cập ngày 16 tháng 4 năm 2018.
- ^ a b “US sodium oxybate label” (PDF). FDA. ngày 16 tháng 11 năm 2017. Truy cập ngày 14 tháng 4 năm 2018. For US label updates see FDA index page for NDA 021196
- ^ a b c d e f g “UK label Summary of Product Characteristics” (bằng tiếng Anh). Electronic Medicines Compendium. ngày 8 tháng 9 năm 2015. Truy cập ngày 14 tháng 4 năm 2018.
- ^ a b c d e “Critical review of gamma-hydroxybutyric acid (GHB)” (PDF). 2012.
- ^ a b “Alcover: Riassunto delle Caratteristiche del Prodotto”. Agenzia Italiana del Farmaco. ngày 31 tháng 3 năm 2017. Index page
- ^ a b “GHB Fact Sheet” (PDF). DEA. Bản gốc (PDF) lưu trữ ngày 6 tháng 5 năm 2017. Truy cập ngày 16 tháng 4 năm 2018.
- ^ a b Wang YG, Swick TJ, Carter LP, Thorpy MJ, Benowitz NL (tháng 8 năm 2009). “Safety overview of postmarketing and clinical experience of sodium oxybate (Xyrem): abuse, misuse, dependence, and diversion”. Journal of Clinical Sleep Medicine. 5 (4): 365–71. PMC 2725257. PMID 19968016.
- ^ a b c Staton, Tracy (ngày 7 tháng 5 năm 2014). “10 big brands keep pumping out big bucks, with a little help from price hikes”. Fierce Pharma. Truy cập ngày 13 tháng 11 năm 2015.
- ^ a b “Press release: US Attorney's Office - Eastern District of New York”. US Department of Justice. ngày 13 tháng 7 năm 2007.
- ^ Alshaikh, Mashael K.; Tricco, Andrea C.; Tashkandi, Mariam; Mamdani, Muhammad; Straus, Sharon E.; BaHammam, Ahmed S. (2012). “Sodium oxybate for narcolepsy with cataplexy: systematic review and meta-analysis”. Journal of Clinical Sleep Medicine. 8 (4): 451–458. doi:10.5664/jcsm.2048. PMC 3407266. PMID 22893778.
- ^ Boscolo-Berto, Rafael; Viel, Guido; Montagnese, Sara; Raduazzo, Daniella I.; Ferrara, Santo D.; Dauvilliers, Yves (2012). “Narcolepsy and effectiveness of gamma-hydroxybutyrate (GHB): a systematic review and meta-analysis of randomized controlled trials”. Sleep Medicine Reviews. 16 (5): 431–43. doi:10.1016/j.smrv.2011.09.001. PMID 22055895.
- ^ Keating, Gillian M. (2014). “Sodium oxybate: a review of its use in alcohol withdrawal syndrome and in the maintenance of abstinence in alcohol dependence”. Clinical Drug Investigation. 34 (1): 63–80. doi:10.1007/s40261-013-0158-x. PMID 24307430.
- ^ Busardò, Francesco Paolo; Kyriakou, Charalampia; Napoletano, S.; Marinelli, Eugene; Zaami, Simona (2015). “Clinical applications of sodium oxybate (GHB): from narcolepsy to alcohol withdrawal syndrome” (PDF). European Review for Medical and Pharmacological Sciences. 19 (23): 4654–4663. PMID 26698265.
- ^ Mannucci, Carmen; Pichini, Simona; Spagnolo, Elvira Ventura; Calapai, Fabrizio; Gangemi, Sebastiano; Navarra, Michele; Calapai, Gioacchino (2018). “Sodium oxybate therapy for the treatment of alcohol withdrawal syndrome and the maintenance of alcohol abstinence”. Current Drug Metabolism. 19. doi:10.2174/1389200219666171207122227. PMID 29219048.
- ^ Abadinsky, Howard (2010). “GHB and GBL”. Drug Use and Abuse: A Comprehensive Introduction (ấn bản thứ 7). Cengage Learning. tr. 197–198. ISBN 9780495809913.
- ^ Miller, Richard Lawrence (2002). The Encyclopedia of Addictive Drugs. Greenwood Publishing Group. tr. 182–185. ISBN 9780313318078.
- ^ Galloway, Gantt P.; Frederick, S. L.; Staggers, Frank E.; Gonzales, Marco; Stalcup, S. Alex; Smith, David E. (1997). “Gamma-hydroxybutyrate: an emerging drug of abuse that causes physical dependence”. Addiction. 92 (1): 89–96. doi:10.1111/j.1360-0443.1997.tb03640.x. PMID 9060200.
- ^ “FDA Approves 'Date-Rape' Drug to Treat Sleep Disorder”. The Washington Post. ngày 18 tháng 7 năm 2002. Truy cập ngày 23 tháng 6 năm 2018.
- ^ Wedin, Gregory P.; Hornfeldt, Carl S.; Ylitalo, Lisa M. (2006). “The clinical development of gamma-hydroxybutyrate (GHB)”. Current Drug Safety. 1 (1): 99–106. doi:10.2174/157488606775252647. PMID 18690919.
- ^ Carter, Lawrence P.; Pardi, Daniel; Gorsline, Jane; Griffiths, Roland R. (2009). “Illicit gamma-hydroxybutyrate (GHB) and pharmaceutical sodium oxybate (Xyrem): differences in characteristics and misuse”. Drug and Alcohol Dependence. 104 (1–2): 1–10. doi:10.1016/j.drugalcdep.2009.04.012. PMC 713368. PMID 19493637.
- ^ Wise, Merrill S.; Arand, Donna L.; Auger, R. Robert; Brooks, Stephen N.; Watson, Natalie F. (2007). “Treatment of narcolepsy and other hypersomnias of central origin: An American Academy of Sleep Medicine Review”. Sleep. 30 (12): 1712–1727. doi:10.1093/sleep/30.12.1712. PMC 2276130. PMID 18246981.
- ^ Lewis, David E. (2012). “Section 4.4.3 Aleksandr Mikhailovich Zaitsev”. Early Russian organic chemists and their legacy. Springer. ISBN 9783642282195.
- ^ Saytzeff, Alexander (1874). “Über die Reduction des Succinylchlorids”. Liebigs Annalen der Chemie (bằng tiếng Đức). 171 (2): 258–290. doi:10.1002/jlac.18741710216.
- ^ Laborit, H; Jouany, JM; Gerard, J; Fabiani, F (1960). “Generalities concernant l'etude experimentale de l'emploi clinique du gamma hydroxybutyrate de Na”. Aggressologie (bằng tiếng Pháp). 1: 397–406. PMID 13758011.
- ^ Centers for Disease Control (ngày 30 tháng 11 năm 1990). “Multistate outbreak of poisonings associated with illicit use of gamma hydroxy butyrate”. MMWR. Morbidity and Mortality Weekly Report. 39 (47): 861–3. PMID 2122223.
- ^ Dyer, JE (tháng 7 năm 1991). “gamma-Hydroxybutyrate: a health-food product producing coma and seizurelike activity”. The American Journal of Emergency Medicine. 9 (4): 321–4. doi:10.1016/0735-6757(91)90050-T. PMID 2054002.
- ^ Institute of Medicine; National Research Council (US) Committee on the Framework for Evaluating the Safety of Dietary Supplements (2002). “Appendix D: Table of Food and Drug Administration Actions on Dietary Supplements”. Proposed Framework for Evaluating the Safety of Dietary Supplements: For Comment (bằng tiếng Anh). National Academies Press (US).
- ^ “GHB: A Club Drug To Watch” (PDF). Substance Abuse Treatment Advisory. 2 (1). tháng 11 năm 2002. Bản gốc (PDF) lưu trữ ngày 1 tháng 8 năm 2017. Truy cập ngày 25 tháng 8 năm 2019.
- ^ Mason, P. E. (2002). “Gamma Hydroxybutyric Acid (GHB) Intoxication”. Academic Emergency Medicine. 9 (7): 730–739. doi:10.1197/aemj.9.7.730. PMID 12093716.
- ^ “Transcript: FDA Peripheral and Central Nervous System Drugs Advisory Committee Meeting”. FDA. ngày 6 tháng 6 năm 2001. Bản gốc lưu trữ ngày 16 tháng 5 năm 2017. Truy cập ngày 25 tháng 8 năm 2019.
- ^ “Jazz Pharma (JAZZ) Announces that Lonza has Terminated Their Sodium Oxybate Supply Agreement”. Street Insider. ngày 25 tháng 3 năm 2010.
- ^ “2000 - Addition of Gamma-Hydroxybutyric Acid to Schedule I”. US Department of Justice via the Federal Register. ngày 13 tháng 3 năm 2000. Bản gốc lưu trữ ngày 1 tháng 5 năm 2021. Truy cập ngày 25 tháng 8 năm 2019.
- ^ “William J. Clinton: Statement on Signing the Hillory J. Farias and Samantha Reid Date-Rape Drug Prohibition Act of 2000”. ngày 18 tháng 2 năm 2000.
- ^ “FDA Approves 'Date-Rape' Drug to Treat Sleep Disorder”. Washington Post. ngày 18 tháng 7 năm 2002.
- ^ “Celltech acquires rights to Xyrem from Orphan Medical - Pharmaceutical”. The Pharma Letter (bằng tiếng Anh). ngày 3 tháng 11 năm 2003.
- ^ “Form S-1/A EX-10.41 Amended and Restated Xyrem License and Distribution Agreement”. www.sec.gov. Jazz Pharmaceuticals vis SEC Edgar. ngày 27 tháng 3 năm 2007. Form S-1/A Index page
- ^ “Celltech sold to Belgian firm in £1.5bn deal”. the Guardian (bằng tiếng Anh). ngày 18 tháng 5 năm 2004.
- ^ “Jazz completes Orphan Medical buy - Pharmaceutical industry news”. The Pharma Letter (bằng tiếng Anh). ngày 4 tháng 7 năm 2005.
- ^ “Press release: Valeant Pharmaceuticals Signs Licensing Agreement for Canadian Rights to (C)Xyrem(R) (Sodium Oxybate) from Jazz Pharmaceuticals. - Free Online Library”. Valeant via Business Wire. ngày 12 tháng 1 năm 2007. Bản gốc lưu trữ ngày 18 tháng 6 năm 2018. Truy cập ngày 25 tháng 8 năm 2019.
- ^ Berenson, Alex (ngày 22 tháng 7 năm 2006). “Indictment of Doctor Tests Drug Marketing Rules”. The New York Times.
- ^ Berenson, Alex (ngày 14 tháng 7 năm 2007). “Maker of Narcolepsy Drug Pleads Guilty in U.S. Case”. The New York Times.
- ^ a b “FDA Warning Letter, Jazz Pharmaceuticals, Inc 10/11/11”.
- ^ The Associated Press (ngày 12 tháng 10 năm 2010). “FDA Says No to Jazz Pharma Fibromyalgia Drug”. The New York Times. Truy cập ngày 12 tháng 10 năm 2010.[liên kết hỏng]
- ^ “2013 - Jazz Pharmaceuticals, Inc.- Close Out Letter” (bằng tiếng Anh). FDA. ngày 2 tháng 8 năm 2013. Bản gốc lưu trữ ngày 13 tháng 1 năm 2017. Truy cập ngày 25 tháng 8 năm 2019.
- ^ “Press release: FDA approves a generic of Xyrem with a REMS Program”. FDA Center for Drug Evaluation and Research (bằng tiếng Anh). ngày 17 tháng 1 năm 2017.
- ^ “This Rival Might Swipe 20% Of Jazz's Sleep Business, But Stock Perks Up | Investor's Business Daily”. Investor's Business Daily. ngày 6 tháng 4 năm 2017. Bản gốc lưu trữ ngày 18 tháng 6 năm 2018. Truy cập ngày 25 tháng 8 năm 2019.
- ^ “8-K”. www.sec.gov. Jazz via SEC Edgar. ngày 5 tháng 4 năm 2017.
- ^ “10-K For the fiscal year ended ngày 31 tháng 12 năm 2017”. Jazz via SEC Edgar. Truy cập ngày 16 tháng 4 năm 2018.
- ^ “Narcolepsy with or without cataplexy in adults: pitolisant | Guidance and guidelines: Other Treatments”. NICE. tháng 3 năm 2017. Truy cập ngày 14 tháng 4 năm 2018.
- ^ Kane, Nancy (tháng 5 năm 2017). “Sodium oxybate for the treatment of narcolepsy with cataplexy in adults” (PDF). NHS Regional Drug & Therapeutics Centre (Newcastle). Bản gốc (PDF) lưu trữ ngày 21 tháng 10 năm 2020. Truy cập ngày 25 tháng 8 năm 2019.
- ^ Rattner, Steven (ngày 30 tháng 6 năm 2013). “An Orphan Jackpot”. The New York Times.
- ^ Danzon PM (Spring 2000). “Making sense of drug prices” (PDF). Regulation. 23 (1): 56–63. Bản gốc (PDF) lưu trữ ngày 11 tháng 10 năm 2012. Truy cập ngày 25 tháng 8 năm 2019.
- ^ “Narcolepsy”. NHS Choices. ngày 29 tháng 5 năm 2016. Truy cập ngày 14 tháng 4 năm 2018.
- ^ “DH funds private prescriptions for drug denied to NHS patients”. Health Service Journal. ngày 20 tháng 7 năm 2015. Truy cập ngày 20 tháng 7 năm 2015.
- ^ “Judge criticises NHS England for 'totally irrational' drug decision”. Health Service Journal. ngày 4 tháng 5 năm 2016. Truy cập ngày 4 tháng 5 năm 2016.
- ^ “Sodium oxybate: CHMP Scientific Discussion” (PDF). EMA. ngày 9 tháng 8 năm 2006. Bản gốc (PDF) lưu trữ ngày 18 tháng 3 năm 2018. Truy cập ngày 25 tháng 8 năm 2019. Linked from EMA index page for EMEA 000593 Lưu trữ 2018-06-20 tại Wayback Machine
- ^ Abad, VC; Guilleminault, C (2017). “New developments in the management of narcolepsy”. Nature and Science of Sleep. 9: 39–57. doi:10.2147/NSS.S103467. PMC 5344488. PMID 28424564.
- ^ de Biase, S; Nilo, A; Gigli, GL; Valente, M (tháng 8 năm 2017). “Investigational therapies for the treatment of narcolepsy”. Expert Opinion on Investigational Drugs. 26 (8): 953–963. doi:10.1080/13543784.2017.1356819. PMID 28726523.
